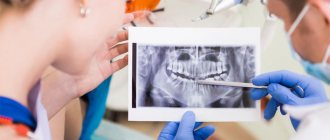
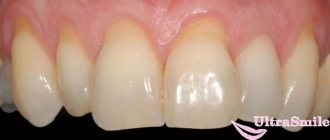
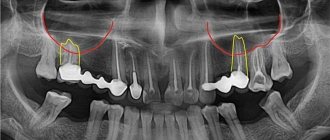
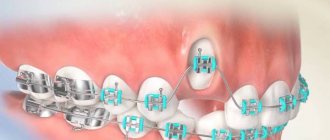
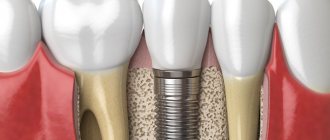
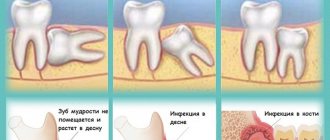
Зубные имплантаты являются одним из наиболее широко используемых методов восстановления отсутствующих зубов. Для этого вы посетите стоматолога, и после осмотра ваш стоматолог может сообщить вам, что перед установкой имплантата требуется костный трансплантат. И это часто пугает пациентов, особенно когда они не знакомы с костными трансплантатами для зубных имплантатов. Но не волнуйтесь, потому что процедура пересадки зубной кости проста и безболезненна. Если вы читаете это, вы, вероятно, являетесь кандидатом на операцию по пересадке костной ткани и хотите узнать об этом больше. Вы пришли в нужное место, потому что в этой статье будет объяснено все, что вам нужно знать о костном трансплантате, включая технику, различные типы трансплантатов, стоимость операции, вероятность успеха, риски и побочные эффекты.
Что такое Зубной костный трансплантат?
Часть челюстной кости может со временем дегенерировать из-за потери одного или нескольких взрослых зубов. В этом случае вам может потребоваться костный трансплантат перед установкой зубного имплантата, чтобы увеличить количество кости в пораженной области челюсти. В целом, операция по пересадке костной ткани зубов-это безболезненная и простая процедура, при которой кость, взятая из любой части тела, срастается с существующей костью челюсти. Эти костные трансплантаты берутся из костей пациента, таких как бедро, бедро или задняя часть челюсти. Это также может быть искусственным. Вы можете спросить: «Необходимы ли зубные костные трансплантаты?»
В ответ на этот вопрос мы должны заявить, что эта операция необходима, если у пациента недостаточно кости в челюсти для поддержки имплантата. Такие факторы, как заболевание десен, травма лица или травма, а также проблемы с развитием, также могут повредить часть челюстной кости, и в этом случае необходима костная пластика.
Также посетите наши продукты для костных трансплантатов: Костный трансплантат Monib
Виды трансплантатов для костной пластики
Натуральный костный материал для костной пластики в условиях современной медицины используется не так часто, как кажется. Инновационные технологии изготовления искусственных трансплантатов позволяют избежать множества недостатков и рисков применения натуральных материалов.
Всего существует четыре вида трансплантатов для проведения костной пластики:
- Аутогенный материал. Трансплантаты, которые берутся из разных участков челюсти, подбородка или твердого неба у самого пациента. Приживается быстрее и удачнее всего, так как не имеет антигенов, на которые среагирует иммунитет человека. Однако установка подобных трансплантатов подразумевает дополнительное вмешательство. В периоде восстановления нужно будет наблюдать за несколькими операционными доступами и ухаживать за ними.
- Аллогенный материал. Натуральный костный материал, который берется от другого человека. Как правило, используются трупы, то есть для применения таких трансплантатов нужны специальные законы, позволяющие забирать какие-либо части тела у умерших людей. Аллогенный материал приживается хуже, но тоже абсолютно безопасен, так как проходит ряд обработок и контролей качества.
- Ксеногенный трансплантат. Материалы животного происхождения в условиях современных технологий пользуются большим успехом. Они изготавливаются из тканей крупного рогатого скота и тщательно модифицируются до подходящей человеку структурной конструкции или стружки. При заполнении пространства таким материалом, врач повышает вероятность повышенной регенерации собственной кости пациента.
- Синтетический материал. Искусственные конструкции широко используются по нескольким причинам. Основной из них является низкая стоимость материала. Кроме того, пациент может 100 % не сомневаться в безопасности трансплантата, созданного синтетическим путем.
В подборе материала для костной пластики участвует пациент, так как финансовая сторона вопроса находится не на последнем месте. Стоматолог обязан подробно разъяснить человеку все особенности натуральных и синтетических трансплантатов, а также порекомендовать наиболее оптимальные варианты.
Как Работает Зубной Костный Трансплантат?
Существует несколько методов выполнения операции по пересадке костной ткани. Однако общий процесс включает в себя то, что стоматолог делает небольшой разрез на челюсти и вставляет костный трансплантат в челюсть. Итак, как работают эти костные трансплантаты или порошки? Костный матрикс находится в скелетной системе. Это твердый материал, который помогает укрепить кости. Матрица формируется и поддерживается живыми костными клетками внутри нее. Врачи соединяют костные трансплантаты, содержащие матрицу и живые клетки, с челюстью. Клетки внутри новой кости могут затем прикрепиться к старой кости. В результате живые костные клетки в костных трансплантатах образуют матрицу и заживляют поврежденную кость. В результате ваша челюстная кость в конечном итоге станет достаточно прочной, чтобы поддерживать имплантат.
Введение
Устранение дефектов челюстей играет одну из ведущих ролей в черепно-челюстно-лицевой хирургии. Костные трансплантаты используются для заполнения костных деформаций и дефектов в черепно-лицевом скелете. Костная ткань — единственная ткань в организме, способная к репаративному остеогенезу без формирования рубца и органотипической регенерации при соблюдении ряда условий. Свободные костные трансплантаты — костные блоки, полученные из донорских зон. В челюстно-лицевой хирургии их принято разделять на внутри- и внеротовые [7, 8]. К внеротовым зонам относят одновременно трансплантаты и из теменных костей, и из малоберцовой кости. Следует признать, что такое разделение несколько условно, поскольку по своему строению и свойствам все типы трансплантатов, включая внутриротовые, имеют между собой достаточное количество отличий, что делает подобное разделение удобным только при планировании оперативного лечения, но не с точки зрения прогноза его эффективности [9, 11, 12].
Метод аутотрансплантации костных блоков широко применяется в таких областях, как травматология и ортопедия, челюстно-лицевая хирургия, реконструктивная хирургия, онкология, нейрохирургия и др. В источниках литературы он фигурирует в качестве «золотого стандарта» в лечении многих заболеваний благодаря возможности получения прогнозируемого клинического результата [3, 17]. Большинство публикаций о высокой эффективности трансплантации костных блоков основывается на клинических и эстетических результатах. Немногочисленные работы, содержащие результаты клинических и гистологических исследований, носят, как правило, описательный характер [4, 19]. Главным механизмом интеграции трансплантированного блока считают остекондуктивные свойства губчатой кости, сохраняющей жизнеспособность. Что касается кортикальной пластинки, то ее роль окончательно не определена [2, 14]. Однако клинические данные указывают на признаки дистрофических изменений в трансплантированных свободных костных балках, что проявляется в снижении минерализации с течением времени [15]. Поскольку замещение обширных дефектов костной ткани свободными трансплантатами связано с риском осложнений, то следующим поколением аутотрансплантатов стали васкуляризированные трансплантаты, или трансплантаты на сосудистой ножке. Они являются частью органа с сохраненной сосудистой сетью, приживаются в ложе и подвергаются интеграции и перестройке под нагрузкой значительно быстрее, чем неваскуляризированные, что объясняется теми же особенностями строения костной ткани [18]. Немногочисленные научные публикации, содержащие результаты гистологических исследований, не проливают свет на механизмы приживления трансплантатов, регенерации, их дальнейшую судьбу [6, 10]. Сравнительный анализ васкуляризированных и неваскуляризированных трансплантатов с применением лучевых и морфологических методов исследований показал, что трансплантат на сосудистой ножке сохраняет способность к удержанию минерального компонента и перестройке трансплантата по типу кортикальной кости в области анастомоза [5, 13, 16].
Таким образом, в настоящее время сложились благоприятные условия для динамического изучения репаративного остеогенеза при аутологичной трансплантации костной ткани.
Типы зубных костных трансплантатов
Еще одной проблемой пациентов является тип зубного костного трансплантата. Потому что для них важны качество и материал трансплантатов, а также процедура. Зубные костные трансплантаты делятся на четыре типа в зависимости от их происхождения и компонентов:
Аллотрансплантаты
Аллотрансплантаты получают из костей другого человека, обычно трупа. Пациенты обычно не предпочитают использовать эти типы трансплантатов, но стоматологи широко используют их сегодня. Сами аллотрансплантаты бывают различных форм, таких как трансплантат с гнездом и трансплантат с сохранением бокового гребня. Основная цель пересадки лунки — избежать атрофии альвеолярной кости. Трансплантат для сохранения бокового гребня используется для расширения челюстной кости для размещения зубного имплантата.
Аутотрансплантаты
Эти типы трансплантатов содержат кости из вашего собственного тела, такие как бедро или челюсть. Блоковый костный трансплантат является известным примером аутотрансплантата. Стоматологи используют этот тип трансплантата, когда в челюстной кости имеются значительные дефекты.
Ксенотрансплантаты
Эти трансплантаты сделаны из костей других видов, таких как коровы, свиньи или кораллы. Стоматологи часто используют эти трансплантаты для лечения дефектов челюстной кости.
Аллопласты
Новейший тип зубного костного трансплантата полностью искусственный и изготовлен из таких соединений, как фосфат кальция или фосфосиликат кальция.
Костная реконструкция: материалы и возможности
История костной аугментации материалами разного происхождения достигает почти столетней глубины. Существенные проблемы, связанные с трансплантационными материалами и усилителями роста, касаются их происхождения, обоснования использования, способа их забора с учетом объема так именуемых биологических «затрат». Еще одна ключевая проблема костных трансплантатов касается аспекта потенциальной «репарации» или регенерации области вмешательства. Репарация представляет собой процесс замены дефектного участка чем-то физически подобным по структуре, но отличающимся биологически и физиологически. Регенерация, напротив, предусматривает использование разных материалов и методов, которые позволяют восстановить биологическую структуру дефектной области полностью идентичной тканью. Хирургам, планирующим проведение аугментации, нужно четко понимать, какой результат они могут прогнозировать по окончании реабилитации, и насколько успешными окажутся применяемые ими техники. Четко понимая все аспекты, врач может достигнуть консенсуса в восстановлении витальной кости, выполненного объема аугментации, скорости заживления и оптимизации процедуры ятрогенного вмешательства.
Направленная регенерация тканей предусматривает реализацию ряда этапов для достижения определенного объема формирования костной ткани в зоне интереса. Данный подход предполагает формирование каркаса, на котором будет формироваться новая ткань. Кровеносные сосуды должны прорасти в формирующуюся область для обеспечения ее питательной среды. Кальций необходим для минерализации органичного матрикса, а остеобласты будут обеспечивать депозицию коллагена, который впоследствии превратится в костную ткань. Сигнализирующие молекулы способствуют притяжению клеток-предшественников (остеобластов, эндотелиальных клеток), которые обеспечивают формирование ткани специфического типа в области интереса. Достижение успешного результата регенерации тканей в челюстно-лицевой области является достаточно сложным процессом, учитывая постоянную активность мышц, наличие вариативных форм бактерий и жидкой среды слюны. Понимание аспектов использования различных трансплантационных костных материалов является важным этапом для достижения необходимого успешного результата в ходе комплексной реабилитации стоматологического пациента.
Рекомендации относительно реконструкции костной ткани
Выбор, стоящий перед хирургом во время процедуры экстракции, выполнения аугментации или синус-лифтинга касается, главным образом, следующих аспектов:
- доступа к области дефекта. Доступ может быть сформирован без сепарации лоскута – миниинвазивно, или же классически – путем сепарации объема окружающих тканей.
- источник костного материала. Аутогенная кость, аллогенные аналоги, аллопласт, ксенотрансплантаты или другие материалы – все они подходят для реконструкции параметров резидуального гребня.
- тип используемого трансплантата. Трансплантат может быть представлен в форме частиц, пасты или блока, разного размера и зернистости, а также могут быть собраны из участков разного происхождения (кортикальной или губчатой части кости).
- специфические характеристики каждого трансплантата. Костные заменители характеризуются различными уровнями минерализации и различной тенденцией к резорбции. следует учитывать, является ли материал остеокондуктивным или остеоиндуктивным и как быстро или медленно, или если вообще подлежит ли он биодеградации.
- тип используемого биологического барьера. Используемые мембраны могут быть синтетическими или коллагеновыми: также они могут быть резорбируемыми или нерезорбируемыми, биологические активными или инертными.
Ранние исследования указывают на то, что в экстракционной лунке, даже без соответствующего использования трансплантата или мембраны, все равно наблюдается формирование витальной костной ткани. Однако полагаться лишь на такой исход не стоит. В 2008 году Fickl и соавторы исследовали различия между разными подходами к экстракции (с и без сепарации лоскута) с дальнейшим заполнением лунки аугментатом или же без выполнения процедуры реконструкции. Они обнаружили, что сепарация тканей слизистой и периоста приводит к большей потере ширины и высоты альвеолярного гребня, по сравнению с теми результатами, которые были получены после реализации миниинвазвиного подхода. Также они отметили факт сохранения первичных размеров кости при заполнении лунки неорганичным трансплантатом бычьего происхождения, чего не отмечалось без проведения процедуры аугментации. Iasella и коллеги, однако, отметили, что более витальная кость формировалась в области постэкстракционных лунок без использованного какого-либо типа графта, хотя потеря изначального объема твердых тканей при этом составляла около 30%. Аналогичных последствий удалось избежать при заполнении лунки минерализованным аллографтом, перекрытым резорбируемой коллагеновой мембраной.
В другом исследовании сравнивали два разных метода аугментации. В лунки устанавливали ксенотрансплантат, полученный из крупного рогатого скота, и перекрывали его резорбируемой мембраной – таким образом удавалось добиться незначительного приросла тканей по высоте, но объем сформированной витальной кости не превышал 26%. Когда же в качестве аналога применяли деминерализованный аллотрансплантат с сульфатом кальция, который перекрывали барьером из сульфата кальция, отмечали аналогичный результат изменения геометрических параметров костного гребня, однако количество витальной кости практически в два раза превышало то, что было отмечено при использовании аллотрансплантата.
Материала для аугментации и изоляции
Сульфат кальция
Сульфат кальция является синтетическим аналогом, который используется во многих конфигурациях в качестве как трансплантата, так и стимулятора роста (фото 1). Исследование, проведенное в 2004 году, продемонстрировало, что данный материал в полугидратной форме без мембраны позволяет отлично сохранить объем тканей, и при этом отмечается приблизительно 60% формирование витальной кости. Новый материал для трансплантации костной ткани, описанный в отчете за 2012 год, является двухфазным и содержит как геми- так и дигидрат кальция сульфата. Этот материал является самоосаждаемым в присутствии крови или слюны, и может использоваться с или без барьерной мембраны. В докладе были представлены гистологические результаты его использования при нескольких типах дефектов, которые свидетельствуют о приросте костной ткани. Кроме того, также удавалось добиться ретенции и увеличения геометрических параметром альвеолярного гребня. Пациентка, изображена на фото 1, обратилась за помощью после значительного абсцесса эндодонтической этиологии, который спровоцировал убыль как вестибулярной, так и язычной костной пластинок. Покрытие двухфазного кальциевого сульфата плотной политетрафторэтиленовой (PTFE) мембраной в течение 3 недель способствовало заживлению участка дефекта. Клинически было очевидно, что объем резиудального гребня удалось сохранить на протяжении более 5 лет, который в свою очередь поддерживал поверх лежащую кератинизированную мягкую ткань (фото 2). Самое главное, что при гистологической оценке было обнаружено 58% витальной костной без остатков гранул костного трансплантата (фото 3).
Фото 1. Процедура аугментации с использованием BPCS и покрытием ПТФЭ-мембраной.
Фото 2. Вид пациента через 5 лет после лечения.
Фото 3. Результаты гистологического исследования демонстрируют 58% витальной кости через 4 месяца после аугментации.
Бета-трикальцийфосфат
Ранее существовали опасения, что трансплантационные материалы, которые полностью резервируются в короткий промежуток времени, могут провоцировать коллапс области проведенной аугментации. Чистый бета-трикальцийфосфат (ß-TCP) (фото 4) был одним из материалов, разработанных для решения этой проблемы. В ходе клинических и гистологических исследований удалось установить, что с его помощью можно обеспечить ретенцию 91% ширины костного гребня, заполняя область дефекта Cerasorb (Curasan, Inc.), и перекрывая участок вмешательства коллагеновыми, либо плотными мембранами из PTFE. Через 4-6 месяцев после аугментации, в область реконструкции были установлены дентальные имплантаты, которые также характеризовали высоким уровнем успешности. У пациента на фото 4, осталось только три зуба на верхней челюсти, которые поддерживали съемный протез. Учитывая специфические условия клинической ситуации было принято решение провести реконструкции резиудального гребня для формирования условий под установку дентальных имплантатов. Через 7 месяцев после заживления участка аугментации, провели сепарацию лоскута (фото 5), и установку имплантата. Было установлено, что аугментат позволил восстановить значительную часть предварительно зарегистрированного дефекта. Анализ полученного образца показал, что тот состоит на 85% из витальной кости в апикальной части, и на 90% в срединном участке, а β-TCP присутствовал только форме тонкой полоски на корональном участке (фото 6).
Фото 4. Бета-трикальцийфофат покрытый коллагеновой мембраной.
Фото 5. Вид через 7 месяцев после лечения в ходе повторного обнажения гребня.
Фото 6. Результаты гистологического исследования демонстрируют значительный объем витальной кости.
TCP (трикальцийфосфат) с покрытием PLGA
Для облегчения использования была разработана упаковка трикальцийфосфата в форме шприцов, материал которых непосредственно может быть использован для аугментации. Подобная система состоит из одного шприца, содержащего 99% β-TCP гранул, покрытых поли лактид-со-гликолидом (PLGA). Содержащие этого шприца смешивают с ампулой, содержащей BioLinker (N-метил-2-пирролидон и воду) (GUIDOR easy-graft, Sunstar) (фото 7). Исследование продемонстрировало биосовместимость и подходящую резорбции этого материала на примерах реконструкции лунок зубов после их удаления. Такой аугментат медленно резорбировался и длительно поддерживал необходимую форму, таким образом на данный момент являясь подходящей альтернативой для костной реконструкции с или без использования мембран. На фото 7 изображено процесс использования данного материала с целью аугментации лунки в области нижнего моляра. Область вмешательства перекрывали коллагеновой мембраной без первичного ушивания раны. Через 8 месяцев в данную область был установлен дентальный имплантата (фото 8). По фото 8 можно заметить, что значительное количество используемого материала резорбировалось и заместилось витальной костной тканью, в то же время удалось сохранить исходные параметры ширины костного гребня.
Фото 7. Упаковка PLGA-TCP в лунку удаленного зуба.
Фото 8. Вид через 8 месяцев после аугментации лунки.
Мембраны
Хотя вопрос об инфицировании и обнажении ПТФЭ-мембран с широкими порами остается еще недостаточно изучен, плотные безпористые аналоги таковых уже многие годы подтверждают свою клиническую эффективность. Использование плотных видов ПТФЭ-мембран (Cytoplast TXT, Osteogenics) для защиты кровяного сгустка по данным многочисленных работ позволяет в значительной степени сохранить исходную ширину альвеолярного хребта. При этом замещение пространства лунок витальной костной тканью по данным рентгенографических и гистологических исследований отмечалось уже через 3 месяца после покрытия областей вмешательства посредством мембран. Аналогично эффективно мембраны могут быть использованы и для покрытия аугментата (фото 1-3). Резорбируемые виды мембран были разработаны для поддержки необходимого объема пространства, учитывая параметры их жесткости и расстояние между внутренним и внешним слоями (GUIDOR Matrix Barrier, Sunstar). Пористый характер поверхностей, состоящих из комбинации эфира лимонной кислоты и полимолочной кислоты, позволяет тканям несколько врасти в мембрану, таким образом обеспечивая более высокий уровень ее стабилизации. При этом частота инфицирования или воспаления тканей вокруг мембран отмечается довольно редко, что аргументирует целесообразность их использования в регенеративной стоматологии, особенно в случаях восстановления дефектов кости вокруг имплантатов или еще до момента их установки. В случае, представленном на фото 9-11 синтетическая мембрана была установлена сразу же после экстракции зуба с дефицитом костной ткани с нёбной стороны. Жесткость мембраны обеспечила формирования такого объема пространства, который являлся необходимым для восстановления определённой конфигурации костного гребня. Через шесть недель участок вмешательства демонстрировал признаки полного заживления без каких-либо следов воспаления или инфицирования. Таким образом также удалось добиться формирования более широкой зоны кератинизировнаных тканей.
Фото 9. Субпериостальная установка мембраны при значительной потере костной ткани со щечной стороны лунки.
Фото 10. Вид окончательно-полученной формы гребня.
Фото 11. Вид через 6 недель после заживления.
Наполнители
Учитывая недостатки порошковых форм аугментатов, некоторые их аналоги были разработаны в виде паст для многофункционального использования: реконструкции области лунок, синус-лифтинга и аугментации костного гребня. Ранее упомянутые BPCS и PLGA / TCP представляют собой как раз такие материалы. Они по сути являются комбинацией деминерализованного / минерализованного аллотрансплантата и коллагенового желатина (Optecure, Exactech), представлял таким образом полужесткий материал для реконструкции костной ткани. По данным производителей данные материала также характеризуются остеоиндуктивностью с возможностью формирования значительных объемов витальной ткани. Пациент на фото 12 обратился за помощью имея во фронтальном участке нижней челюсти ширину кости приблизительно в 1 мм. Аллографт смешивали со стерильном физиологическом растворе, и перекрывали сульфатом кальция (3D Bond, Augma Biomaterials) и мембраной Ossix Plus (Datum Dental Ltd). Имплантаты узкого диаметра (ANEW, Dentatus) были установлены 4 месяца спустя. Клинический результат лечения изображен на фото 13, представляя собой вид через 3 года после нагрузки установленных имплантатов.
Фото 12. Вид участка дефицита костной ткани во фронтальном участке нижней челюсти.
Фото 13. Вид через 3 года поле протезирования.
Неорганический трансплантат бычьего происхождения
В ранних исследованиях процедуры синус-лифтинга использования неорганический костный трансплантат бычьего происхождения. Во многих публикациях описывали применения данного ксенографта как изолировано, так и вместе с аутогенной костной тканью, или даже с определенными факторами роста. Когда ксенографт использовали изолировано, но перекрывали его мембраной, процент формирования витальной кости составлял от 12% до 17% в течение 6-10 месяцев после операции. В другом исследовании ксенографт применяли вместе с факторами роста для поднятия уровня Шнейдеровой мембраны. Результаты данного мультицентричного исследования с участием 25 пациентов продемонстрировали, что формирование костной ткани через 6 месяцев составляло около 50%, что более эффективно не только с позиции прироста тканей, но и с позиции времени, потраченного на реабилитацию.
Выводы
В обсуждении результатов гистологического исследования области реконструкции лунки зуба посредством полугидрата сульфата кальция Guarneri и коллеги утверждали следящее: «Цель любой процедуры аугментации — добиться формирования 100% живой костной ткани, окружающей имплантаты». В зависимости от размера и местоположения дефекта, специфики взаимосвязи с окружающими тканями данная цель может быть достигнутой, или же наоборот – невозможной для достижения. Согласно долгосрочным исследованиям успеха имплантатов, установленных в область аугментации, наличие в области вмешательства невитальных частиц трансплантата никаким образом не компрометирует успешность лечения. Исследования же, описывающие опыт применения резорбируемых мембран, указывают на возможность немедленной установки имплантатов при аргументированном выборе метода аугментации. Материалы для восстановления объема костного гребня, а также для изоляции области реконструкции обеспечивают врача различными возможностями для адаптации хирургического подхода в ходе комплексной реабилитации пациента. Определив конечную цель процедуры, и спрогнозировав возможны ее результат через 3, 6, 9 или более месяцев, врач может более доказательно подойти к выбору алгоритма вмешательства, основывая на предварительных данных, описанных в респектабельных научных источниках.
Авторы: Robert A. Horowitz, DDS Minas D. Leventis, DDS, MS, PhD Michael D. Rohrer, DDS, MS Hari S. Prasad, BS, MDT
Лучший Кандидат На Имплантацию Зубной Кости
Возможно ли установить зубной имплантат без костного трансплантата? Вопрос хороший, и ответ-да. Зубные имплантаты не всегда требуют операции по пересадке костной ткани. Это возможно, когда вы идете к стоматологу сразу после потери зуба. Однако, если вы подождете несколько месяцев, челюстная кость на месте отсутствующего зуба начнет разрушаться. В этих условиях вам понадобится костный трансплантат перед установкой зубного имплантата. Зубные костные трансплантаты предназначены не только для имплантатов. Эта операция необходима при таких обстоятельствах, как заболевания десен, травмы и травмы челюстной кости, а также аномалии развития. В результате выбор опытного стоматолога и использование качественных костных трансплантатов позволяют провести операцию без осложнений.
Центр трансплантации костного мозга клиники «Анадолу»
На базе нашего медицинского центра с 2010 года функционирует специализированный центр пересадки костного мозга. В среднем врачи «Анадолу» проводят 250 пересадок в год у пациентов от 16 лет и старше.
В состав центра входят амбулатория, клиническое отделение трансплантации костного мозга и три лаборатории: генетического типирования, гемофореза, криоконсервации и обработки стволовых клеток. Наши специалисты — высококвалифицированные трансплантологи и гематологи, владеющие всеми современными методиками пересадки костного мозга. В своей работе они неукоснительно следуют международным протоколам лечения онкологических заболеваний крови и соблюдают все меры предосторожности и безопасности.
Отделение трансплантации костного мозга «Анадолу» работает не только с международным, но и турецким банком костного мозга, который позволяет максимально быстро — всего за несколько недель — подобрать подходящего донора. В мировом регистре этот процесс может занимать несколько месяцев.
Материал подготовлен по согласованию с врачом медицинского профессором Зафером Гюльбашем.
Отторжение Костного Трансплантата Зуба
Еще одной проблемой пациентов является отказ зубных костных трансплантатов. Вы можете спросить, возможно ли это? Хотя вероятность успеха имплантации зубной кости составляет примерно 99,3%, может произойти сбой. Но что вызывает эту неудачу? Здесь задействовано несколько факторов, но основной причиной отказа костного трансплантата является операция по пересадке кости, выполненная неопытным хирургом. Но это может случиться и с профессиональными хирургами. Отторжение или отказ костного трансплантата может произойти по следующим причинам:
- Если материал для костной пластики заражен бактериями, процедура завершится неудачей;
- Инфекция хирургических инструментов может привести к переносу бактерий в место операции и отторжению трансплантата.;
- Неудача возможна, если пациент неправильно соблюдает послеоперационный уход, предписанный хирургом,
- Если вы не соблюдаете надлежащую гигиену полости рта после операции, у вас могут возникнуть проблемы.
Симптомы Отторжения одного Зубного Трансплантата
Отторжение костных трансплантатов может происходить на ранней и поздней стадиях, каждая из которых имеет свои собственные симптомы. В течение трех — четырех месяцев после операции у вас могут возникнуть ранние сбои. В этом случае могут возникнуть следующие симптомы, и вам следует немедленно посетить своего стоматолога:
- Отек костного трансплантата зуба: Через несколько дней после операции часто наблюдается отек в области операции и части лица. Однако, если отек длится более нескольких недель или усиливается, это признак того, что ваше тело отторгает костный трансплантат.
- Острая боль: Через несколько дней после операции боль и отек являются нормальными, потому что боль при имплантации костной ткани является одним из наиболее распространенных побочных эффектов этой операции. Однако, если боль сохраняется и усиливается с течением времени, это может указывать на то, что костный трансплантат не удался.
- Большие объемы утечки: как и при других операциях, ожидается некоторый дренаж из обрабатываемой области. Однако, если утечка сохраняется и происходит большой объем дренирования, это один из важнейших симптомов отказа трансплантата, и вам следует немедленно обратиться к врачу.
- Заболевание десен: Если у вас постоянная инфекция десен в течение трех или четырех месяцев после операции, это может указывать на проблему с вашим лечением.
Это были признаки ранней неудачи костного трансплантата, но иногда эта неудача может произойти через 6-12 месяцев после операции. Симптомы поздней стадии недостаточности различны, и вам следует обратить внимание на то, связано ли это с отторжением трансплантата или другим заболеванием. Эти симптомы включают следующее:
- Бактериальная инфекция во рту, которая поражает десны и другие зубы;
- Если состояние вашей полости рта ухудшается, несмотря на серьезный и регулярный уход;
- Вы заметили, что стискиваете зубы намного сильнее, чем обычно;
- Если вы заметили, что ткань десен отступает или что объем кости вокруг места операции со временем уменьшается, обратитесь к своему стоматологу;
- Вы можете чувствовать давление на имплантат, когда едите или жуете
- Вы страдаете от боли в шее или голове.
В результате после любой операции рекомендуется постоянная бдительность в течение многих лет. Если вы осознаете эти симптомы и вовремя обратитесь к врачу, вы сможете предотвратить многие заболевания полости рта, которые могут вас беспокоить. Обратившись к специалисту как можно скорее, ваш хирург сможет предложить подходящее решение проблемы. Однако даже небольшая задержка может иметь необратимые компенсирующие последствия.
Альтернатива натуральному материалу
Современная медицина постоянно создает синтетические конструкции разного применения. В стоматологии активно модернизируются синтетические трансплантаты, которые гораздо дешевле по себестоимости, но не уступают характеристиками натуральным материалам. Рекомендуется использовать наиболее современные и проверенные виды синтетических трансплантатов, ведь они лучше всего приживаются.
Некоторые стоматологи полностью отказываются от натурального костного материала для костной пластики и закупают искусственные трансплантаты. Чаще всего они имеют гранулированную форму, что позволяет быстро отрегулировать объем восстановления кости. Отсутствие органической составляющей в материале снижает иммунную несовместимость и минимизирует процессы отторжения. Нередко именно применение синтетических трансплантатов позволяет одномоментно провести имплантацию и прочно зафиксировать искусственные корни для будущих коронок.
Риски при имплантации Костной Ткани
Костный трансплантат для зубных имплантатов-это простая и, как правило, малорисковая операция. Однако пациенты всегда обеспокоены рисками и побочными эффектами этой операции и готовы узнать о ней больше. Как правило, операции могут иметь некоторые осложнения, некоторые легкие, а некоторые очень тяжелые. Тяжесть побочных эффектов зависит от различных факторов, таких как опыт хирурга, использование качественных материалов и физиология пациента. Хотя операция по пересадке костной ткани является процедурой с низким уровнем риска, у вас могут возникнуть некоторые из следующих побочных эффектов, которые являются нормальными:
- Легкое кровотечение из десен, которое может длиться в течение нескольких дней;
- Отек десен и части лица, который восстанавливается через несколько дней;
- Трудности с едой, речью и жеванием,
- Пиан
Это распространенные побочные эффекты, которые все пациенты испытывают через три-четыре дня после операции. Однако в редких случаях могут возникнуть серьезные осложнения при имплантации костной ткани, которые могут иметь опасные последствия для пациента. Возможные осложнения включают:
- Сильное кровотечение и инфекция в области операции;
- Воспаление, отек и мучительный дискомфорт;
- Повреждение нервов частей лица или десен во время операции;
- Неблагоприятная реакция на анестезию, которая может возникнуть во время или после операции;
- Ваше тело может отторгнуть пересаженную кость;
Но помните, что эти осложнения редки и могут возникнуть менее чем у 1% пациентов. Кроме того, тщательно выбирая своего хирурга и принимая необходимые меры предосторожности после операции, вы можете значительно снизить вероятность серьезных побочных эффектов.
Как проводится операция?
Пересадка костных блоков, как правило, происходит не в стационаре, а стоматологическом кабинете. Все манипуляции выполняются под местной анестезией – боли во время операции пациент не чувствует.
Костный блок необходимого размера и объема устанавливают в том участке челюсти, где имеется дефицит костной ткани. Фиксируют трансплантат с помощью винтов, изготовленных из титана или оксида циркония – биологически нейтральных материалов. Пересаженный фрагмент закрывают специальной защитной мембраной, настилают сверху лоскут мягких тканей и накладывают швы.
В собственной кости, с которой соприкасается трансплантат, делают небольшие отверстия, через которые прорастают новые кровеносные сосуды. В течение полугода они пронизывают костный блок, и он становится частью организма. После прочного сращения подсаженной кости с родной выполняется имплантация. Имплантат, внедренный в восстановленную кость, может прослужить столько же, сколько имплантат, установленный в натуральную кость.
Во время костной пластики пациент не испытывает никакого дискомфорта – он находится по седацией. В послеоперационном периоде возможно появление болевых ощущений, которые купируются при помощи обезболивающих препаратов. Появление отеков и синяков предупреждают прикладыванием льда к месту операции.
Время Восстановления после Операции по пересадке Костной Ткани
Период восстановления после операции по пересадке костной ткани может составлять от двух недель до трех месяцев, в зависимости от таких факторов, как тип операции и физическая сила пациента. Однако для заживления костного трансплантата потребуется три месяца. Некоторые пациенты возобновляют свою обычную деятельность через две недели после операции, в то время как другим может потребоваться 6-12 месяцев для восстановления. Послеоперационный уход необходим, и если вы будете делать это осторожно, у вас будет более короткий период восстановления. Вот несколько этапов заживления костного трансплантата, которые помогут вам быстро восстановиться:
- У вас будет легкое кровотечение через 12-24 часа после операции. Чтобы остановить это, положите марлевую салфетку в область операции и немного прикусите; держите ее в таком положении в течение часа.
- Припухлость вокруг рта, подбородка, глаз и некоторых частей лица является нормальной. Используйте пакет со льдом, чтобы уменьшить отек в течение 48 часов с интервалом в 30 минут.
- Завершите прием лекарств, назначенных вашим врачом, таких как обезболивающие и антибиотики.
- Избегайте интенсивной деятельности в течение двух недель после операции, так как это может вызвать кровотечение.
- Следует избегать курения в течение одного месяца до операции и в период заживления, поскольку курение задерживает процесс заживления и развитие новых костных тканей.
- В первые несколько дней после операции придерживайтесь мягкой диеты со средней температурой, чтобы избежать повреждения области операции.
Результаты
Гистологическая структура костных регенератов после трансплантации блоков ветви нижней челюсти
При гистологическом исследовании костных трепанобиоптатов из области трансплантации свободным трансплантатом было выявлено, что костная ткань состоит из хорошо выраженной кортикальной пластинки и губчатой кости. Межбалочное пространство заполнено ретикулярной стромой костного мозга без очагов кроветворения и с участками грубоволокнистой неоформленной соединительной ткани. Костный массив кортикальной кости имел пластинчатое строение с хорошо выраженными гаверсовыми каналами. Часть трабекул состояла из неоднородного костного матрикса — внутренняя структура трабекулы была представлена костным матриксом с пустыми лакунами с щелями и расслоенными участками костного вещества (см. рис. 1, а). На поверхности балок располагалась костная ткань с остеоцитами, иногда незрелая. Внутренняя поверхность гаверсовых каналов и наружная поверхность части трабекул имели признаки гладкой резорбции — разволокнение костного вещества с изменением тинкториальных свойств красителя. Межбалочное пространство было заполнено неоформленной рыхловолокнистой соединительной тканью регенераторного типа. В свою очередь трабекулы губчатой кости трансплантата с сохраненной жизнеспособностью имели зрелую структуру, местами на поверхности обнаруживали образование остеоида и пролиферирующие остеобласты. Остеокластическая активность была заметна по наличию эрозивных поверхностей на поверхности костных балок. В отличие от кортикальной пластинки трабекулы несли на себе остеокласты в умеренном количестве. Гаверсовы каналы часто были без сосудов. В ряде случаев весь столбик трепанобиоптата был представлен некротизированной костью.
При морфометрическом исследовании обращало на себя внимание наличие двух вариантов костных структур в следующих пропорциях: некротизированной кости (BDV/CV=9,76±1,04%) и жизнеспособной, в том числе новообразованной костной ткани (BTV/CV=45,07±3,88%). Ткань межбалочного пространства была представлена желтым костным мозгом (MaV/CV=40,08±5,84%) и неоформленной плотноволокнистой соединительной тканью (Fb.V/CV=3,67±0,57%).
Процессы остеогенеза протекали как на поверхности трансплантата, сохранившего жизнеспособность, так и, в большей мере, на поверхности костных структур с признаками некроза. Явления остеорезорбции имели место по механизму гладкой и остеокластической резорбции, причем на поверхности некротизированных участков трансплантации остеоклазия превалировала (Ra.Oc=15,6±1,5%). Оценка костного баланса показала преобладающий вклад в регенеративный остеогенез трансплантата новообразованной костной ткани с сохранившейся жизнеспособностью (BB-BT=5,6±1,8) по сравнению с некротизированными участками (BB-BD=2,54±0,75) на данном сроке наблюдения.
По данным мультиспиральной компьютерной томографии (МСКТ), проведенной через 4 мес после трансплантации свободного костного блока ветви нижней челюсти, при исследовании поперечных и аксиальных срезов обращало на себя внимание умеренное снижение костной плотности трансплантата по сравнению с кортикальной пластинкой альвеолярного отростка ветви нижней челюсти. Выраженного слияния воспринимающего ложа с трансплантатом не происходило (см. рис. 1, б).
Гистологическая структура костных регенератов после трансплантации блоков подвздошной кости на сосудистой ножке
При гистологическом исследовании трепанобиоптатов, полученных из костного трансплантата, через 12 и 24 мес после аутотрансплантации фрагмента подвздошной кости определили, что костная ткань столбика на начальном этапе состояла из кортикальной пластинки и лежащей под ней губчатой кости. Кортикальная пластинка была умеренной толщины, трабекулы губчатой кости — крупные, широкие. Межтрабекулярное пространство было заполнено красным костным мозгом, иногда с признаками замещения желтым костным мозгом. Кортикальная пластинка часто имела крупные гаверсовы каналы, которые были выстланы эндостом. В них наблюдалась ретикулярная строма костного мозга, переходящая в желтый костный мозг. Трабекулы губчатой кости были также покрыты эндостом, имели признаки остеокластической резорбции с образованием характерных лакунарных выемок, остеобластическая активность была умеренной (рис. 2, а).
Рис. 2. Дезорганизация костного матрикса трансплантированного костного блока ветки нижней челюсти через 4 мес после операции. Окраска по Папаниколау. ×400 (а). Снижение минеральной плотности костной ткани трансплантата по данным МСКТ через 4 мес (б). Через 24 мес межтрабекулярное пространство лишь местами было заполнено красным костным мозгом. Трабекулы трансплантата были утолщены за счет напластования новообразованной костной ткани. Признаки остеоклазии имели место как на костном веществе трансплантата, так и на поверхности новообразованной кости.
При морфометрическом исследовании также наблюдалось наличие двух вариантов костных структур: некротизированной кости (BDV/CV=5,7±1,5%) и жизнеспособной, в том числе в новообразованной костной ткани (BTV/CV=48±3,75%). Ткань межбалочного пространства была представлена желтым костным мозгом (MaV/CV=38,8±7,4%). Оценка костного баланса (ВВ) продемонстрировала преобладающий вклад в регенеративный остеогенез новообразованной костной ткани (BB=44,2±5,8) по сравнению с трансплантатом и его некротизированных участков на данном сроке наблюдения. Явления остеорезорбции определялись по механизму как гладкой, так и остеокластической резорбции (Ra.Oc=36%). Процессы остеогенеза и остеоклазии на поверхности трансплантата и некротизированной кости завершились образованием вокруг них пластинчатого костного матрикса.
При МСКТ-исследовании поперечных и аксиальных срезов нижней челюсти после пластики костным блоком на сосудистой ножке из ветви гребня подвздошной кости спустя 12 мес после трансплантации наблюдалось формирование артифициальной нижней челюсти путем интеграции и перестройки костного трансплантата с начальными признаками формирования кортикальной пластинки и хорошо выраженным губчатым веществом. Костная плотность артифициальной челюсти была сопоставима с контралатеральной половиной (см. рис. 3, б).
Рис. 3. Костный регенерат через 12 мес после трансплантации блока подвздошной кости на сосудистой ножке. Окраска по Массону. ×200 (а). МСКТ области трансплантации: через 6 мес плотность костной ткани в трансплантате сопоставима с костями скелета, не вовлеченными в процесс (б).
Гистологическая структура костных регенератов после трансплантации свободных блоков теменной кости с костной крошкой
По данным гистологического исследования трепанобиоптатов, полученных от пациентов после остеопластики трансплантатами аутологичной теменной кости, костная ткань была представлена рыхлой кортикальной пластинкой, под которой располагался слой губчатой кости. Кортикальная пластинка узкая, узурирована фолькмановыми каналами. Костные трабекулы губчатой кости были местами узкими, местами нормальной толщины. Костная ткань трабекул с небольшими участками неокончательно минерализованной костной ткани (рис. 4, а).
Рис. 4. Трепанобиоптат из костного регенерата через 12 мес после трансплантации блока теменной кости в сочетании с костной крошкой из теменной кости. Окраска по Папаниколау. ×200 (а). Формирование костных структур артифициальной челюсти из трансплантата по данным МСКТ через 12 мес после операции (б). На поверхности трабекул обнаруживали остеобласты округлой или кубической формы, с базофильным ядром и ядрышком, в окружении остеоида или лежащих на поверхности свободно. В большинстве своем трабекулы были очагово выстланы уплощенными клетками — предшественниками остеобластов, находящихся в покое. В некоторых местах регистрировалась остеокластическая активность, сопровождающаяся гладкой резорбцией поверхности костной балки. Межбалочное пространство было заполнено ретикулярной нежно-волокнистой соединительной тканью и умеренно васкуляризировано. Ретикулярная строма не содержала жировой и кровеносной тканей. Межбалочное пространство в кортикальном слое с некоторым фиброзом.
При морфометрическом исследовании было выявлено наличие двух вариантов костных структур в следующих пропорциях в трепанобиоптатах спустя 6 мес после операции: некротизированной кости (BDV/CV=5,7±1,5%) и жизнеспособной, в том числе новообразованной костной ткани (BTV/CV=48±3,75%). Ткань межбалочного пространства была представлена желтым костным мозгом (MaV/CV=38,8±7,4%). Через 12 мес некротизированную часть трансплантата определяли по немногочисленным островкам костной ткани, расположенным в центре костных структур. Идентифицировать ткань трансплантата не представлялось возможным. Относительный объем костной ткани (BV/CV) составил 72,4±5,4%. Ретикулярная строма не содержала кроветворные элементы. Остеорезорбция через 6 мес после трансплантации осуществлялась по механизму остеокластической резорбции (Ra.Oc=14±3,8%). Через 12 мес наблюдалось снижение резорбционной активности (Ra.Oc=12±5%). Оценка костного баланса (ВВ) показала, что больший вклад в регенеративный остеогенез вносила новообразованная костная ткань (BB=44,5±8,6), чем трансплантат и его некротизированные участки. Репаративный остеогенез через 12 мес сохранял свою активность (BB=25,7±7,6).
Результаты МСКТ через 6 мес после трансплантации костных блоков теменной кости и костной крошки: при исследовании поперечных и аксиальных срезов нижней челюсти было зафиксировано, что структура нижней челюсти в месте трансплантации анатомически соответствует структуре кости с контралатеральной стороны, выражены кортикальная пластинка и губчатое вещество. Костная плотность была сопоставима с противоположной стороной (см. рис. 4, б).
Гистологическая структура костных регенератов после трансплантации васкуляризированных блоков малоберцовой кости
При гистологическом исследовании трепанобиоптатов, полученных из трансплантата малоберцовой кости, через 6, 12 и 24 мес после трансплантации было выявлено, что столбик трепана в основном состоял из плотного массива костной ткани, который мог соответствовать кортикальной пластине трубчатой кости. Гаверсовы каналы были миндалевидными, имели тенденцию к расширению с течением времени. На ранних сроках в просвете гаверсовых каналов наблюдались только сосуды и ретикулярная строма костного мозга, которая с течением времени дополнялась новообразованной костной тканью, к 24 мес просветы были частично заполнены новообразованной костной тканью. Процесс резорбции трансплантата начинался по типу гладкой резорбции путем набухания и разволокнения матрикса, что меняло его текториальные свойства при полихромных окрасках. Остеокласты на ранних сроках были единичны. Остеобластическая активность минимальна и представлена единичными остеобластами. Через 12 мес после трансплантации гаверсовы каналы были расширены, часто неправильной формы, ветвились, что напоминало губчатую кость. В области физиологической перестройки кости обнаруживались единичные остеокласты. Остеобластическая активность была минимальной и представлена немногочисленными остеобластами в участках реверсии (рис. 5, а).
Рис. 5. Трепанобиоптат из костного регенерата через 12 мес после трансплантации блока малоберцовой кости на сосудистой ножке. Окраска по Папаниколау. ×200 (а). Умеренное снижение минеральной плотности костной ткани трансплантата по данным МСКТ через 12 мес после трансплантации. Через 24 мес в просвете гаверсовых каналов определялись ретикулярная строма костного мозга и сосуды, содержащие форменные элементы, а также костные структуры, напоминающие губчатую костную ткань. В некоторых случаях встречались скопления клеток кроветворной ткани. Трабекулы были неравномерно распределены в пространстве, толщина их значительно различалась как по толщине столбика, так и по его длине. Внутренняя поверхность гаверсова канала с эндостальной выстилкой, переходящей на костные структуры внутри каналов, часто наблюдались признаки остеокластической резорбции. Единичные остеокласты выявлялись в области физиологической перестройки кости. Остеобластическая активность была минимальной и представлена немногочисленными остеобластами в участках реверсии на поверхности как трансплантата, так и новообразованной кости внутри гаверсовых каналов. Костное вещество содержало остеоциты с базофильным ядром, часть лакун остеоцитов не имела клеток, особенно в отдалении от кровеносных сосудов. Костные пластинки в костном веществе преимущественно сохраняли характерный рисунок, соответствующий пластинчатой костной ткани кортикальной пластинки трубчатой кости — остеонные структуры с циркулярными пластинками, немногочисленными вставочными пластинками (рис. 6, а).
Рис. 6. Трепанобиоптат из костного регенерата через 24 мес после трансплантации блока малоберцовой кости на сосудистой ножке. Окраска по Папаниколау. ×200 (а). Формирование кортикальных пластин и губчатого вещества в трансплантате по данным МСКТ через 24 мес после трансплантации (б).
Таким образом, микроскопическая картина в динамике соответствовала переживающему трансплантату, частично некротизированному, с признаками перестройки костной ткани в начале по типу гладкой, а позднее 1 года по остеокластическому типу, а также признаками репаративного остеогенеза внутри просветов гаверсовых каналов с формированием неорганизованного костного вещества и иногда с фокусами кроветворения.
При морфометрическом исследовании также определялись два варианта костных структур в следующих пропорциях в образцах через 6 мес после трансплантации: частично некротизированной кости (BDV/CV=42±7,5%) и жизнеспособной, в том числе новообразованной костной ткани (BTV/CV=22±9,75%). Ткань межбалочного пространства была представлена желтым костным мозгом (MaV/CV=33,4±8,2%). Спустя 12 мес после трансплантации относительная объемная доля костной ткани сократилась преимущественно за счет резорбции некротизированной кости (BDV/CV=18±4,1%, BTV/CV=27±3,7%). Через 24 мес после трансплантации относительная объемная доля костной ткани имела тенденцию к росту преимущественно за счет резорбции трансплантата и образования костной ткани (BDV/CV=23,7±4,4%, BTV/CV=37±5,9%).
Динамика репаративного остеогенеза в переживающем трансплантате складывалась из полугодового периода относительной стагнации (BB=2,25±0,6, Ra. Oc=5,7%±0,3%), характеризовалась некоторым умеренным всплеском регенерации к 12 мес на фоне выраженной остеорезорбции (BB=3±0,3, Ra. Oc=7,2±0,6%) и последующим замедлением остеогенеза к 24 мес на фоне продолжающейся резорбции (BB=1,5±0,03, Ra. Oc=9,4%±0,8%).
При КТ-исследовании поперечных и аксиальных срезов нижней челюсти пациентов после пластики малоберцовыми трансплантатами было выявлено, что структура трансплантата изменялась, начиная с 12 мес (см. рис. 5, б). Если в этот период структура трансплантата полностью повторяла малоберцовую кость по анатомической структуре и костной плотности, то к 24 мес происходило истончение кортикальной пластинки, увеличение размеров артифициальной челюсти, расширение размеров трансплантата с изменением соотношения кортикальной пластинки и губчатой кости в пользу последней. Костная плотность была сопоставима с противоположной стороной (см. рис. 6, б).
Сколько Стоит Зубной Костный Трансплантат?
Стоимость операции по пересадке костной ткани зубов варьируется в зависимости от различных факторов, включая географическое положение пациента, тип применяемого трансплантата и другие медицинские процедуры. Средняя стоимость составляет от 200 до 1300 долларов за трансплантат. Эта стоимость указана только для искусственных костных трансплантатов. Таким образом, пациентам, которым требуется костный аутотрансплантат, придется платить больше, потому что в этих обстоятельствах будет проведена дополнительная процедура. В целом, стоимость зубных костных трансплантатов очень разумна, и поэтому мы советуем пациентам не откладывать выполнение этой операции.
Недостатки трансплантации костных блоков
Самый главный недостаток процедуры в том, что это хирургическая операция со всеми вытекающими отсюда последствиями: дополнительными тратами, длительной реабилитацией и отсрочкой непосредственно установки имплантов и протезов, поскольку должно пройти от 2 и более месяцев для полного восстановления нарощенной костной ткани.
Можно ли провести имплантацию без трансплантации блоков?
У процедуры есть небольшое количество альтернатив. Первая – это расщепление челюстного гребня. Кость разрезается вдоль по горизонтали, ее края раздвигаются, а промежуток заполняется материалом собственной донорской кости, либо искусственной костью. Это более сложная к проведению операция – трансплантация блоков переносится гораздо легче.
Существуют также методы имплантации без наращивания костной ткани. Но у них тоже есть свои ограничения и противопоказания, в особенности это касается очень узкой костной ткани – ее попросту не хватит для фиксации имплантатов. Конечно, существуют тонкие модели, специально рассчитанные на узкую кость. Но подбираются они строго индивидуально.
Операции по трансплантации костных блоков в проводятся опытными челюстно-лицевыми хирургами. Именно от профессионализма врача во многом зависит отсутствие осложнений после процедуры и ее эффективность. Нашим клиентам мы гарантируем профессиональный подход и бережное отношение.
1 Перова М.Д. Осложнения дентальной имплантации, их лечение и профилактика. Новое в стоматологии. 2002.
резюме
Зубной костный трансплантат-это простая процедура, используемая для замены отсутствующей челюстной кости. В этом методе хирурги используют различные типы костных трансплантатов в соответствии с потребностями пациента и серьезностью проблемы. Когда необходима операция по пересадке костной ткани? Если вы знаете, как делаются зубные имплантаты, вы поймете важность операции по пересадке костной ткани. В челюсти должно быть достаточно кости, чтобы удерживать штифты имплантата на месте, чтобы зуб был надежно закреплен. Поэтому использование костных трансплантатов имеет важное значение для роста костей в целевой области. Если вы также являетесь кандидатом на операцию по пересадке костной ткани и у вас есть вопросы по определенной теме, напишите нам, чтобы мы могли вас направить.