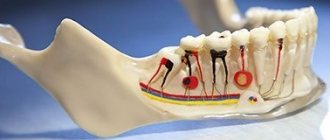
Кератокиста
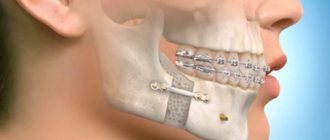
В Центре челюстно-лицевой хирургии и имплантологии проводится лечение и удаление такого доброкачественного образования верхней или нижней челюсти как кератокиста.
Что такое челюстные кисты, причины их появления и симптоматика
Профилактика и лечение заболеваний зубов пропагандируется с раннего детства, поэтому большинство из нас ответственно подходит к этому вопросу. Однако мало кто знает, что в ротовой полости могут возникать и другие проблемы, которые часто требуют хирургического вмешательства. Речь идет о челюстных кистах. Согласно статистике, это совсем не редкое явление и множество пациентов обращается к стоматологам с такого рода проблемами. Что же собой представляет киста челюсти и как следует лечить данную патологию? Виды и особенности кист челюстей Киста представляет собой тканевую полость, которая выстлана изнутри эпителием и заполнена жидкостью. Возникает такое новообразование в результате дегенерации ткани прорезывающихся зубов или тех зубов, которые только развиваются. Согласно медицинским данным, киста нижней челюсти встречается в три раза реже, чем киста верхней челюсти. При этом как киста нижней челюсти, так и киста верхней челюсти может привести к таким неприятным последствиям, как остеомиелит, поэтому лечить кисту нужно обязательно. В стоматологии диагностируют три вида кист челюсти: радикулярную кисту челюсти, фолликулярную и примордиальную кисту челюсти (кератокисту).
Речь идет о кисте нижней челюсти, возникающей на месте образования зуба мудрости. Она представляет собой мягкое тканевое образование с тонкими стенками, заполненное особенным веществом — холестеатомой. Такая киста может быть многокамерной или однокамерной.
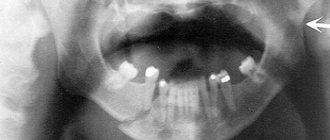
Ее появление обычно протекает бессимптомно, не вызывает болезненности или дискомфорта, и чаще всего обнаруживается врачом случайно при проведении рентгенологического исследования по какому-то иному поводу. Киста может развиваться довольно длительное время от нескольких месяцев до нескольких лет не вызывать беспокойства. Тем не менее, при обнаружении этого новообразования необходимо провести соответствующее лечение, иначе киста может со временем увеличиться в размерах, множиться, стать источником инфекции ротовой полости, воспалиться, а также послужить причиной разрушения (рассасывания) челюстной кости.
Лечение челюстных кист
На начальных стадиях развития кератокисты может быть достаточно электролечения, и врач-терапевт назначит процедуру депофорез. При значительных размерах кисты необходимо хирургическое вмешательство, которое проводится под местной или общей анестезией.
Для лечения челюстных кист стоматологи прибегают к оперативному лечению. Проводя цистостомию и цистэктомию, иногда корневые кисты хорошо поддаются лечению без оперативных вмешательств. Но осложнения кист и их нагноения требуют обязательного вскрытия с последующим дренированием полости.
Основная задача хирургического лечения — сохранить зубы, которые находятся в зоне кисты, и восстановить их нарушенные функции. Цистэктомия помимо вскрытия полости кисты позволяет одномоментно произвести резекцию корня зуба. Эту процедуру проводят, если корень зуба погружен в полость кисты не более, чем на 1/3 всей его длины. Если же погружение более глубокое, то зубы становятся непригодными с точки зрения функциональности и довольно рано выпадают. Основной недостаток этого метода в том, что после резекции, снижается функциональность зубов, отмечаются случаи реинфекции со стороны срезанных микроканальцев, кроме этого операция довольно травматична. Костные полости, которые остаются после резекции снижают прочность челюстных костей. Современные технологии позволяют улучшить процедуру цистэктомии. Биокомпозитный материал, которым заполняют костную полость, предотвращает возникновение ранних осложнений. Это связано с отсутствием кровяного сгустка, что значительно снижает инфицирование полости. Биокомпозитные материалы, заполняя полость кисты, способствуют восстановлению формы и функций челюсти за счет ускорения регенерации.
Прогноз после оперативного лечения благоприятный, однако, крупные челюстные кисты могут осложняться патологическими переломами челюсти.
В Центре челюстно-лицевой хирургии и имплантологии эта операция проводится хирургами высшей категории с использованием самого современного оборудования и новейших анестезирующих препаратов. В сложных случаях послеоперационная реабилитация может быть проведена в условиях собственного стационара, которым располагает Центр. Уютные палаты, комфортные условия и постоянное медицинское наблюдение сделают период восстановления легким и приятным для пациента.
Дифференциальная трехмерная диагностика кератокист челюстей
М. А. Чибисова
д. м. н., профессор, ректор, заведующая кафедрой рентгенологии в стоматологии ЧОУ «СПбИНСТОМ» (Санкт-Петербург), председатель секции СтАР «Лучевая диагностика в стоматологии»
А. А. Зубарева
д. м. н., профессор кафедры оториноларингологии с клиникой ПСПбГМУ им. акад. И. П. Павлова, профессор кафедры рентгенологии в стоматологии СПбИНСТОМ (Санкт-Петербург)
А. Л. Дударев
д. м. н., профессор кафедры рентгенологии в стоматологии СпбИНСТОМ (Санкт-Петербург)
А. В. Холин
д. м. н., профессор, заведующий кафедрой лучевой диагностики СЗГМУ им. И. И. Мечникова (Санкт-Петербург)
Е. В. Кайзеров
ассистент кафедры лучевой диагностики СЗГМУ им. И. И. Мечникова (Санкт-Петербург)
Р. Х. Чарыев
аспирант кафедры челюстно-лицевой хирургии и хирургической стоматологии ПСПбГМУ им. акад. И. П. Павлова (Санкт-Петербург)
Резюме
Применение современных методов лучевой диагностики обосновано также в послеоперационном периоде для динамического анализа восстановительного периода пациентов с кератокистами челюстей. Использование современных высокотехнологичных методов лучевой диагностики, таких как цифровая ортопантомография (ОПТ, ОПТГ), спиральная (МСКТ) и конусно-лучевая компьютерная томография с динамической денситометрией (КЛКТ, 3ДКТ, 3DКТ), наряду с детальным анализом клинических и гистологических данных позволяет значительно повысить качество оценки состояния зубочелюстной системы в норме и при выявлении патологических процессов. Трехмерная томография (МСКТ и КЛКТ) позволяет провести дифференциальную диагностику между типами кистозных образований, проанализировать степень распространения патологического процесса на окружающие ткани и определить наиболее походящий способ оперативного вмешательства, в том числе у пациентов с кертокистами челюстей.
Ключевые слова:
кератокиста, одонтогенные кисты челюстей, конусно-лучевая компьютерная томография (КЛКТ, 3ДКТ, 3DКТ), мультиспиральная рентгеновская компьютерная томография (МСКТ).
Введение
Кератокисты челюстей, по данным различных авторов, составляют от 5.4 до 17.4 % из всех одонтогенных кист [2, 5, 11]. В специализированных стоматологических учреждениях до 10 % пациентов находятся по поводу лечения кератокист челюстей. Кератокисты склонны к рецидивированию, которое возникает в результате неполного удаления эпителиальной оболочки кисты. Причиной рецидивов также является высокая активность коллагеназы в стенке кисты и высокая фибринолитическая активность [1, 2].
Кератокиста относится к группе одонтогенных дизэмбриогенетических кист (международная гистологическая классификация одонтогенных опухолей, кист и других опухолеподобных образований челюстных костей ВОЗ, Женева, 1972), является пороком развития челюстно-лицевой области, образуется в результате нарушения дифференцировки эпителия эмалевого органа в период онтогенеза, гистологически представляет собой костную полость выстланную кератинизированным многослойным эпителием [2, 6, 7, 11].
Несмотря на стремительное развитие методов лучевой диагностики в последние десятилетия, появление спиральной КТ, а также конусно-лучевой дентальной объемной томографии, нет четких дифференциально-диагностических критериев для определения характера кистозного образования челюстей [8, 9]. Основным рутинным методом лучевой диагностики в стоматологии по-прежнему остается ортопантомография и ее цифровое усовершенствование, которые, безусловно, позволяют получить массу полезной информации по состоянию зубочелюстной системы, в том числе и для оценки кистозных образований [10]. Однако, при преимуществах ОПТГ как массового, экономически обоснованного и достаточно информативного метода лучевой диагностики в стоматологии, имеется ряд ограничений и погрешностей данного метода, не позволяющих достоверно интерпретировать все возможные рентгенологические признаки кистозного образования [1—5].
Рис. 1. Кератокиста угла и ветви ниж- ней челюсти слева. МСКТ. Рис. 2. Кератокиста тела, угла и ветви нижней челюсти. Четкий неровный внешний контур, дольчатое строение, псевдоперегородки. 3DКТ. Рис. 3. Кератокиста тела, угла и ветви нижней челюсти с распространением на мыщелковый и венечный отростки. Размер 63 мм. МСКТ.
Гистологически существует два варианта строения кератокисты: паракератозный и ортокератозный. Паракератозный вариант является наиболее распространенным, наиболее агрессивным по темпам роста и деструкции костной ткани, а также по частоте рецидивов, представлен 5—7 слоями эпителия с характерным базальным слоем, клетки которого — кубической или цилиндрической формы с вертикальным расположением гиперхромных ядер. Стенка кисты представлена рыхлой соединительной тканью с отеком подэпителиальных отделов без воспалительной инфильтрации. При ортокератозном варианте эпителий более утолщенный, без четко выраженного базального слоя, с обширной зоной поверхностного отдела в состоянии истинного кератоза [11].
Цель исследования
Целью нашего исследования явилась разработка дифференциально-диагностических клинико-рентгенологических критериев для постановки диагноза «кератокиста» с использованием клинических данных стоматологического обследования пациента, а также возможностей методов компьютерной томографии, таких как денситометрия содержимого кистозной полости, окружающей костной ткани и мягких тканей челюстной области в перифокальной зоне, степень деструкции губчатого костного вещества челюстей, кортикальных пластин, метрические показатели кистозной полости в трех измерениях, направление роста кисты, связь с зубами, сосудисто-нервными структурами челюстей. Полученные данные могут быть использованы для оптимального выбора метода лечения, объема хирургического вмешательства с целью максимально возможного сохранения челюстной кости, височно-нижнечелюстного сустава, зубов, предотвращения повреждения сосудисто-нервных образований челюстей.
Рис. 4. Содержимое кератокисты: мягкотканный компонент + воздух. Обширный дефект вестибулярной кортикальной пластинки тела нижней челюсти. МСКТ. Рис. 5. Погружение интактных корней в кисту. МСКТ.
Материалы и методы
Были проанализированы результаты клинического и компьютерно-томографического обследования (цифровой ОПТГ, МСКТ и дентальной объемной томографии) 46 пациентов с кератокистами челюстей, подтвержденными данными цитогистологического исследования. Анализ проводили по трем формализованным картам: клинической (жалобы, анамнез, данные объективного обследования), 3D-РКТ-кистограмме (рентгеносемиотика кератокист), локальной денситометрии в различных зонах (использование единиц HU для МСКТ и УЕ для дентальной объемной томографии). Данная группа пациентов оценивалась по следующим клиническим и рентгенологическим критериям: распределение частоты встречаемости кератокист в различных возрастных группах, распределение по половому признаку, данные анамнеза заболевания (давность возникновения кисты, темпы ее роста, связь с кариозными зубами, болезненность), локализация в различных отделах нижней челюсти, деформация челюсти, состояние слизистой оболочки, десневых карманов, наличие зубов в проекции кисты и состояние их корней, метрические характеристики кератокист в трех измерениях, денситометрические характеристики содержимого кисты, капсулы и окружающих костных структур и мягких тканей, состояние окружающей костной ткани, наличие дефектов кортикальных пластинок, воздействие на нижнечелюстной канал, височно-нижнечелюстной сустав.
Результаты и обсуждение
Таблица № 1. Распределение кератокист по возрасту у мужчин
| Возраст | Абс. (n-25) | % |
| 10—20 | 4 | 16 |
| 21—30 | 3 | 12 |
| 31—40 | 6 | 24 |
| 41—50 | 3 | 12 |
| 51—60 | 6 | 24 |
| 61—70 | 2 | 8 |
| 71—80 | 1 | 4 |
Таблица № 2. Распределение кератокист по возрасту у женщин
| Возраст | Абс. (n-21) | % |
| 10—20 | 1 | 4.8 |
| 21—30 | 6 | 28.6 |
| 31—40 | 6 | 28.6 |
| 41—50 | 1 | 4.8 |
| 51—60 | 1 | 4.8 |
| 61—70 | 4 | 19 |
| 71—80 | 2 | 9.5 |
Данные таблиц № 1 и 2 демонстрируют, что кератокисты были диагностированы у мужчин в возрасте от 11 до 74 лет (25 случаев) и у женщин в возрасте от 13 до 76 лет (21 случай). Наибольшая частота встречаемости кератокист у мужчин приходится на возраст 30 до 60 лет — 15 (60 %), у женщин — от 20 до 40 лет — 12 (57.2 %).
Таблица № 3.
Клиническая симптоматика кератокист
| Симптомы | Количество наблюдений | ||
| Абс. (n-46) | % | ||
| Жалобы | Отсутствие жалоб, кистозная полость выявлялась при плановом лучевом обследовании | 16 | 34.8 |
| Жалобы на вздутие и деформацию нижней челюсти | 30 | 65.2 | |
| Боль при открывании рта | 6 | 13 | |
| Данные объективного стоматологического обследования | Вздутие челюсти по переходной складке | 30 | 65.2 |
| Скудное гнойное отделяемое из десневых карманов. | 6 | 13 | |
| Адентия в проекции кератокисты | 23 | 50 | |
| Патологическая подвижность зубов в проекции кисты | 20 | 43.5 | |
| При пальпации истончение кортикальных пластинок нижней челюсти, их крепитация | 19 | 41.3 | |
| При пальпации дефекты кортикальных пластинок нижней челюсти | 9 | 19.6 | |
| Электроодонтометрия зубов в проекции кисты соответствовала интактным зубам (2—6 мкА) | 42 | 91.3 | |
| Показатели электроодонтометрии отклонялись от нормы (6—20 мкА) | 4 | 8.7 | |
| Сопутствующая воспалительная патология | Гингивит | 1 | 2.2 |
| Невралгия тройничного нерва | 3 | 6.5 | |
Как показывают данные таблицы № 3
, в трети случаев, 16 (34.8 %), жалобы отсутствовали. Диагноз устанавливался при рентгенологическом обследовании. Характерными были жалобы на вздутие и деформацию челюсти — 30 (65.2 %). Жалобы на болевые ощущения предъявляли только 6 (13 %) пациентов. Характерными признаками при стоматологическом обследовании являлись вздутие челюсти по переходной складке — 30 (65.2 %), адентия в проекции кисты — 23 (50 %), патологическая подвижность зубов в проекции кисты — 20 (43.5 %), крепитация — 19 (41.3 %) и дефекты кортикальных пластинок — 9 (19.6 %) при пальпации. Данные электроодонтометрии в 42 (91.3 %) случаях соответствовали нормативным значениям. Не зафиксировано ни одного случая глубокого кариеса зубов в проекции кисты.
На этапе лучевой диагностики с использованием цифровой ОПТГ, спиральной КТ и дентальной объемной томографии получены следующие данные.
Таблица № 4. Синдромно-симптомная рентгеновская компьютерно-томографическая характеристика кератокист челюстей
| РКТ-симптомы | Количество наблюдений | ||
| Абс. (n-46) | % | ||
| Локализация | Тело нижней челюсти на уровне премоляров | 4 | 8.7 |
| Тело нижней челюсти на уровне моляров | 6 | 13 | |
| Угол нижней челюсти | 8 | 17.4 | |
| Ветвь нижней челюсти | 5 | 10.9 | |
| Тело, угол и ветвь нижней челюсти | 9 | 19.6 | |
| Тело и угол нижней челюсти | 7 | 15.2 | |
| Угол и ветвь нижней челюсти | 6 | 13 | |
| Форма | однокамерная | 15 | 32.6 |
| многокамерная | 5 | 10.9 | |
| дольчатая | 26 | 56.5 | |
| Размеры | <10 мм | 5 | 10.9 |
| 10—30 мм | 12 | 26.1 | |
| >30 мм | 29 | 63 | |
| Контуры | Внутренние: | ||
| Ровные | 17 | 37 | |
| Неровные | 29 | 63 | |
| Четкие | 39 | 84.8 | |
| Нечеткие | 7 | 15.2 | |
| Внешние: | 7 | 17 | |
| Ровные | 19 | 41.3 | |
| Неровные | 27 | 58.7 | |
| Четкие | 39 | 84.8 | |
| Нечеткие | 7 | 15.2 | |
| Склерозированные | 7 | 15.2 | |
| Структура | Однородная: | 21 | 45.7 |
| Жироподобная ткань | 4 | 8.7 | |
| Жидкость | 5 | 10.9 | |
| Мягкие ткани | 12 | 26.1 | |
| Неоднородная: | 25 | 54.3 | |
| Жироподобная ткань + воздух | 6 | 13 | |
| Фиброзная ткань + воздух | 2 | 4.3 | |
| Мягкие ткани + воздух | 8 | 17.4 | |
| Жидкость + воздух | 4 | 8.7 | |
| Мягкие ткани + фиброзная ткань + воздух | 5 | 10.9 | |
| Состояние окружающих тканей | Оттеснение нижнечелюстного канала | 19 | 41.3 |
| Дефект стенки нижнечелюстного канала | 13 | 28.3 | |
| Уплотнение окружающих мягких тканей | 5 | 10.9 | |
| Наличие фиброзной капсулы | 25 | 54.3 | |
| Адентия в проекции кисты | 23 | 50 | |
| Погружение корня в кистозную полость | 12 | 26.1 | |
| Лизис корней зубов в проекции кисты | 5 | 10.9 | |
| Дивергенция корней зубов в проекции кисты | 7 | 15.2 | |
| Вздутие челюсти | 30 | 65.2 | |
| Истончение кортикальных пластинок | 46 | 100 | |
| Дефект кортикальных пластинок | 37 | 80.4 | |
| Направление роста кисты | По длинной оси челюсти с распространением на 1 зуб | 5 | 10.9 |
| По длинной оси челюсти с распространением на 2 зуба | 12 | 26.1 | |
| По длинной оси челюсти с распространением на 3 и более зубов | 29 | 63 | |
| По длинной оси челюсти с распространением на венечный и мыщелковый отростки | 3 | 6.5 | |
Данные таблицы № 4 демонстрируют, что типичной локализацией кератокист являлись тело нижней челюсти на уровне премоляров и моляров, угол и ветвь нижней челюсти, причем за счет больших размеров кератокиста распространялась на два — 13 (28.3 %) — или три отдела нижней челюсти — 9 (19.6 %), а в трех случаях достигала мыщелкового и венечного отростков (6.5 %).
Для кератокист характерно дольчатое строение кистозной полости — 26 (56.5 %) с псевдоперегородками, которые образованы кератиновыми массами (рис. 1—2). Однокамерное строение наблюдалось при малых размерах кистозной полости (при размерах менее 10 мм в 100 % случаях, при размерах 10—30 мм в 30 % случаев).
В наблюдениях преобладали кератокисты размером более 30 мм — 29 (63 %), размером 10—30 мм — 12 (26.1 %). Кистозная полость размером менее 10 мм встречалась в 5 наблюдениях (10.9 %).
Внутренние контуры кисты и в большинстве случаев четкие — 39 (84.8 %), неровные — 29 (63 %). Внешние контуры кисты также в большинстве случаев были четкими — 39 (84.8 %), неровными — 27 (58.7 %).
Более чем в половине наблюдений выявлено неоднородное содержимое кератокист — 25 (54.3 %). Среди кератокист с однородным содержимым преобладал мягкотканный компонент — 12 (26.1 %) (рис. 3
—
4).
Характерным являлось вздутие нижней челюсти, которое наблюдалось у 2/3 обследуемых, — 30 (65.2 %) с истончением — 46 (100 %) и дефектами — 37 (80.4 %) кортикальных пластинок (рис. 5
). Часто встречающимся признаком кератокисты нижней челюсти являлось оттеснение — 19 (41.3 %) или частичное разрушение — 13 (28.3 %) — стенки нижнечелюстного канала.
Характерно направление роста кератокисты по длинной оси нижней челюсти с распространением на 3 и более зубов — 29 (63 %). Погружение корня в кистозную полость наблюдалось у 12 (26.1 %) пациентов (рис. 5). В 5 (10.9 %) случаях наблюдался частичный лизис корня, погруженного в кисту. В зоне кератокисты у половины пациентов — 23 (50 %) — определялась вторичная адентия.
Таблица № 5. Денситометрические характеристики содержимого кератокист
| Структура | Рентгеновская плотность | Количество наблюдений | ||
| HU | у. е. | абс. (n-46) | % | |
| Однородная | 21 | 45.7 | ||
| Жироподобная ткань | От -30 до -180 | 1350—1450 | 4 | 8.7 |
| Жидкость | От 13 до 17 | 1300—1400 | 5 | 10.9 |
| Мягкие ткани | От 25 до 40 | 1350—1500 | 12 | 26.1 |
| Неоднородная: | 25 | 54.3 | ||
| Жироподобная ткань + воздух | От -30 до -180, -1000 | 1350—1450, 650—950 | 6 | 13 |
| Фиброзная ткань + воздух | От 56 до 69, -1000 | 650—950 | 2 | 4.3 |
| Мягкие ткани + воздух | От 25 до 40, -1000 | 1350—1500, 650—950 | 8 | 17.4 |
| Жидкость + воздух | От 13 до 17, -1000 | 1300—1400, 650—950 | 4 | 8.7 |
| Мягкие ткани + фиброзная ткань + воздух | От 25 до 40, от 56 до 69, -1000 | 1350—1500, 1400—1550 650—950 | 5 | 10.9 |
Наряду с изучением особенностей 3D-РКТ-изображений кератокист мы проводили изучение количественных денситометрических показателей. В таблице № 5
демонстрируется, что, по данным локальной денситометрии, содержимое кератокист было представлено жироподобным — 4 (8.7 %), жидкостным — 5 (10.9 %) и мягкотканным компонентом — 12 (26.1 %). Более чем в половине случаев содержимое было неоднородным, с примесью воздуха — 25 (54.3 %).
Заключение
Спиральная компьютерная томография и дентальная объемная томография (КЛКТ), с учетом клинических особенностей развития кератокист, позволяют получить более полную информацию о кистозном образовании челюстей за счет возможности трехмерной визуализации, оценки размеров и локализации без погрешностей, связанных с укладкой пациента и проекционными искажениями, более точной оценки состояния кортикальных пластинок на разных уровнях в разных проекциях с целью точного определения кортикальных дефектов. Данные методы позволяют получить детальную информацию о взаимоотношении кистозной полости и таких важных анатомических структур, как нижнечелюстной канал, мыщелковый отросток. Использование локальной денситометрии позволяет количественно оценить содержимое кистозной полости, состояние капсулы, окружающей костной ткани и мягких тканей, признаки наличия остеорепаративных процессов, а также состояние корней зубов, вовлеченных в патологический процесс.
Выводы
Итогом нашего исследования явилась разработка детальной клинико-лучевой семиотики кератокист нижней челюсти с использованием рентгенологических симптомов, денситометрических данных и данных клинического обследования.
В результате исследования можно сделать выводы о том, что кератокисты чаще встречаются в молодом возрасте, локализуются преимущественно в области тела, угла и ветви нижней челюсти на уровне моляров, не имеют ярких клинических проявлений, за исключением постепенно нарастающей деформации челюсти, имеют большие размеры, неправильную форму за счет распространения по длинной оси челюсти и высокой остеолитической активности, не связаны с кариозными зубами, хотя могут вызывать лизис корней зубов, приводят к образованию обширных дефектов кортикальных пластинок, склонны к оттеснению и лизису стенок нижнечелюстного канала.
Микрохирургические операции челюстно-лицевой хирургии
Микрохирургия — универсальный метод, применяемый практически во всех хирургических дисциплинах для устранения дефекта той или иной ткани. В организме человека существуют более 400 донорских участков с осевым типом кровоснабжения, откуда забрав ткань, не наносится никакого вреда дальнейшему кровоснабжению всего органа. В реконструкции челюстей основное место играет свойство лоскута с наличием такого количества и качества кости, которое позволит воссоздать анатомическую целостность твердых тканей и в дальнейшем возможность применения для дентальной имплантации и протезирования.
Для тотальных и субтотальных дефектов нижней челюсти предпочтителен малоберцовый кожно-костный лоскут. Малоберцовая кость обладает достаточно большими опорными свойствами, имея в наличие достаточно большое количество кортикального компонента, и легко поддается моделированию для воссоздания анатомических контуров. Подвздошный или по-другому паховый кожно-костный лоскут оптимален для реконструкции небольших дефектов нижней челюсти, в последних случаях возможно иногда применение свободной подвздошной кости.
Для тотальных и субтотальных дефектов верхней челюсти оптимальны лучевой кожно-костный и малоберцовый кожно-костный лоскуты. В тех случаях, когда дефект охватывает скуло-верхнечелюстной контрфорс в сочетании с дефектом альвеолярного отростка, возможно выполнить восполнение костного дефекта кортикально-губчатыми теменными трансплантатами и нижнечелюстными, взятыми с ветви и подбородочной области свободными трансплантатами, обладающими мезенхимальным происхождением, что оптимально для реконструкции средней зоны лица.
Безусловно, доминантной остается алгоритм, направленный на приживление лоскута на сосудистой ножке. Если приходится выбирать между удобством для последующей дентальной имплантации в виде наличия кортикальной пластинки костного компонента аутотрансплантата в области воссозданного альвеолярного отростка для последующей имплантации и от этого коим или иным образом снижается надежность работы сосудистого анастомоза, необходимо выбирать надежность приживления. Часто возникают споры между хирургами-имплантологами и реконструктивными хирургами о том, как должна располагаться в области дефекта подвздошная кость, однако опыт показывает, что компромиссов не может быть, поскольку при тромбозе сосудистого анастомоза, теряется весь лоскут. Необходимо также понимать, что расположение губчатого компонента в области альвеолярного отростка не мешает последующей имплантации, поскольку в течение 6 месяцев происходит образование новой.
Для возвращения и нормализации функции жевания и способности питаться необходимо наличие:
- 1. Губ и комплекса органов глотания.
- 2. Наличие челюстей.
- 3. Наличие зубов и прикус, обеспечивающий адекватное жевание.
- 4. Наличие контрфорсов.
- 5. Стабилизация ВНЧС.
- 6. Синхронность работы жевательных мышц.
- 7. Психическое равновесие пациента.
В литературе мы не нашли определенного алгоритма или подходов, направленных на возвращение таких жизненно важных способностей как сосание и глотание, жевание и нормализация речевой функции. Для нормализации питания пациента необходимо наличие губ, в противном случае происходит слюнотечение с последующей мацерацией кожи и невозможность приема и отправления пищи в пищевод. Пациенты с дефектами мягких тканей приротовой области постоянно страдают гастритами, воспалительными явлениями ротоглотки, поскольку вакуумное свойство эвакуации пищи в пищевод снижено, многие адаптируются глотать с открытым ртом, запрокидывая голову назад, у последних усвоение углеводов нарушено, поскольку слюна принимает участие в очищении полости рта от остатков пищи, налета и бактерий, благодаря буферным свойствам, она нейтрализует отрицательное действие сильных кислот и щелочей в пределах емкости буфера, обеспечивает поступление ионов, необходимых для реминерализации зубов, обладает противобактериальными, противогрибковыми и противовирусными свойствами. Клод Бернар доказал, что мы распознаем функции органа, выявляя последствия его отсутствия. С точки зрения функционального возвращения способности питаться второе место нашего алгоритма занимает наличие челюстей. Для устранения дефектов части или всей челюсти мы применяем предоперационное планирование.
Предоперационное планирование челюстей ведется при помощи 3D визуализирующих программ, позволяющих моделировать размеры и формы аутотрансплантатов с учетом позиционирования мыщелковых отростков нижней челюсти в височных ямках (в переднее-верхнее положение в суставных впадинах) по КТ-сканам. Несмотря на то, что мы выполняем реконструкцию в прежнем прикусе, чаще всего приходится сталкиваться с уже ремоделированным ВНЧС и нарушенным прикусом. Поэтому необходимо планирование с учетом последующего достижения центральной окклюзии в центральном соотношении. Функциональное исследование окклюзии заключается в сравнении центральной окклюзии (ЦО- окклюзия при которой наблюдается максимальный контакт между зубами верхней и нижней челюсти) и центрального соотношения (ЦС-состояние, при которой головки нижней челюсти занимают переднее-верхнее положение в суставных впадинах). В случае существенной разницы необходимо описание различий. Так существенная разница между этими состояниями чаще встречается при асимметричных деформациях и при деформациях II-го класса по Энглю. Определение ЦС важно для правильного составления операционного плана.
При планировании устранения верхнечелюстных дефектов, мы учитываем необходимость восстановления контрфорсов, а также воздухоносность верхней челюсти. Контрфорсы являются важнейшей составляющей для опоры альвеолярного отростка, в противном случае после протезирования возникает подвижность верхней челюсти.
Хотя восстановление утраченной гайморовой полости и слизистой выстилки не является возможным, необходимо восстановление анатомической близости, поэтому заполнение скуловерхнечелюстного контрфорса подвздошной костью является некорректным. Оптимально использование свободных расщепланных нижнечелюстных или теменных аутокостных блоков по форме в комбинации с костью на сосудистом питании. В дальнейшем, возможно, с развитием технологий применения стволовых клеток, мы научимся восстанавливать и истинную слизистую выстилку верхнечелюстных или околоносовых пазух.
В реконструкции верхней челюсти мы используем малоберцовый аутотрансплантат для реконструкции тотальных дефектов и лучевой при субтотальных. При использовании лучевого кожно-костного лоскута в последующем для постановки дентальных имплантатов возникает необходимость воссоздания второго кортикально-губчатого слоя альвеолярного отростка с лингвальной стороны, что возможно сделать при помощи теменных или нижнечелюстных свободных аутоблоков.
В челюстно-лицевой микрохирургии при необходимости воссоздания изгибов костей, в выборе трансплантатов с наличием кости мы ограничены подвздошным, малоберцовым, лучевым лоскутами, поскольку лишь последние позволяют 3 D моделирование костного компонента конгруентно дефекту.
Чаще всего даже при оптимальном выборе трансплантата, проведении всех диагностических мероприятий, мы сталкиваемся с дизокклюзией при устранении субтотальных дефектов челюстей, поскольку до сих пор в стране остается открытой проблема одномоментной реконструкции после резекции. Необходимо понимать, что если реконструкция выполняется не одномоментно с резекцией челюсти и даже не накладывается временная титановая конструкция для поддержания прикуса, происходит ремоделирование височно-нижнечелюстного сустава как со здоровой, так и со стороны патологии и нарушение трофики жевательной мускулатуры. В этих случаях до постановки дентальных имплантатов и до протезирования прижившегося трансплантата, выполняется ортодонтическая фиксация прикуса в виде применения брекет-систем и мини-имплантатов, а также миорелаксация жевательных мышц со стороны здоровой челюсти в применении Ботекс-терапии или миотроника.
ИСТОРИЯ ПРОБЛЕМЫ
Микрохирургическая аутотрансплантация в целях реконструкции челюстей в своем развитии на наш взгляд прошла несколько этапов:
1-й этап – качественное взятие аутотрансплантата, минимальное ее моделирование, и перенос в реципиентную зону. Основной задачей этого этапа было обеспечение приживления трансплантата (с 1978 – 1990 гг).
2-й этап — включал в себя более качественное моделирование аутотрансплантатов с использованием обычных рентгенограмм и восковых шаблонов. Основной задачей этого этапа являлось восстановление эстетики лица. Нарушенная функция нижней челюсти восстанавливалась после ряда дополнительных коррегирующих операций и съемного протезирования зубов (с 1990-1995 гг.). 3 этап — компьютерное моделирование нижней челюсти и восстановление жевательной функции при помощи протезирования с использованием дентальных имплантатов. Основной задачей этого этапа является восстановление эстетики лица и жевательной функции нижней челюсти без использования дополнительных корригирующих операций (с 1995 – 2011 гг.). 4 этап — восстановление не только идеального прикуса и стабилизации ВНЧС, но и устранение дисбаланса жевательной мускулатуры (собственно данная статья и открывает 4-й этап истории челюстно-лицевой микрохирургии).
Нами разработан алгоритм лечения пациентов с дефектами челюстей: 1. Предоперационное 3 D планирование и изготовление стереолитографических и накусных шаблонов. Планирование с учетом последующей дентальной имплантации и протезирования. Выбор оптимального лоскута. 2. Восстановление контрфорсов при возможности, анатомических контуров альвеолярного отростка челюстей при помощи свободных и на сосудистой ножке костных трансплантатов. 3. Ремоделирование ВНЧС при устранении субтотальных дефектов нижней челюсти. 4. Дентальная имплантация и протезирование.
Микрохирургическая операция: резекция нижней челюсти, пораженной опухолью с одномоментной реконструкцией малоберцовым трансплантантом на сосудистой ножке
| 1. Резекция нижней челюсти, пораженной опухолью в пределах здоровых тканей | ||
| 2. Этап контроля резекции по предоперационному шаблону | ||
| 3. Забор малоберцовой кости на сосудистой ножке | ||
| 4. Этап моделирования забранного трансплантанта с использованием авторского прибора Караяна А.С. и Назаряна Д.Н. | ||
| 5. Контроль смоделированного трансплантанта на предперационном шаблоне | ||
| 6. Фиксация трансплантанта на сосудистой ножке к оставшимся здоровым фрагментам нижней челюсти | ||
| 7. Микрохирургический этап: под микроскопом ушиваются сосуды с голени и наружная сонная артерия, яремная вена, после сшивания сосудов снимаюются клипсы и ткани, взятые с ноги наполняются кровью, т.е. лоскут становится живым, но уже на челюсти. | ||
| 8. Контроль кровенаполнения — завершающий этап микроскопической операции | Смотреть видео | |
| 9. Внешний вид пациентки до и после операции будет практически неизменным, благодаря одномоментной реконструкции через 6 месяцев человек будет полностью реабилитирован | ||
В научно-клиническом отделе челюстно-лицевой и пластической хирургии ФГБУ НКЦО ФМБА России под руководством профессора Караяна А.С. и к.м.н. Назаряна Д.Н. выполняются уникальные операции по устранению дефектов челюстей. Подобные операции выполняются лишь в 3-х медицинских центрах России.
Одонтогенные кисты челюстей
Одонтогенные кисты челюстей являются весьма распространенной патологией. В настоящее время хирургическое лечение данной патологии является наиболее эффективным, так как все одонтогенные околокорневые кисты являются хроническими очагами инфекции, оказывающей неблагоприятное воздействие на организм. Одонтогенные кисты — внутрикостные полостные образования, появление которых обусловлено либо нарушением развития зубного фолликула, либо хроническим воспалительным процессом в периодонте. Киста состоит из оболочки, полости, в которой находится опалесцирующая жидкость с кристаллами холестерина.
По морфо- и патогенезу , а также локализации различаются следующие виды кист: 1. Кисты, образующиеся из эпителия зубообразующей пластинки (радикулярные ) : -периодонтальная -боковая периодонтальная -резидуальная (остаточная) 2. Кисты, развивающиеся из эмалевого органа или фолликула : -фолликулярная -примордиальная -гингивальная 3. Кисты, развивающиеся из эмалевого органа или островков Маляссе : -кератокиста Клиническая картина: -жалобы могут отсутствовать, а киста может явиться случайной находкой при рентгенологическом обследовании -при увеличении размеров кисты может возникать деформация челюсти и возникает выбухание слизистой оболочки — при увеличении размеров кисты в проекции жевательной группы зубов на верхней челюсти, киста может прилегать, оттеснять, проникать в верхнечелюстную пазуху. В связи с чем могут беспокоить головная боль,чувство тяжести в средней зоне лица на стороне поражения, затруднение носового дыхания ( в том числе при прорастании кисты в нижний носовой ход) -при локализации кисты на нижней челюсти по мере ее роста может возникать компрессия нижнего луночкового нерва, что может привести к онемению на коже и слизистой оболочке нижней губы и подбородка, возможно зубов, на стороне поражения (симптом Венсана). При значительном увеличении размеров кисты возможно возникновение патологического перелома на нижней челюсти. -обострение процесса может привести к нагноению кисты. Как правило, появляется отек мягких тканей, в некоторых случаях затрудненное открывание рта ( если киста располагается в проекции третьих моляров), при внутриротовом обследовании отмечается гиперемия слизистой оболочки, симптом флюктуации (зыбление), болезненность при дотрагивании, возможна патологическая подвижность причинного зуба. Диагностика: 1.внутриротовая контактная рентгенограмма 2.ортопантомограмма 3.рентгенограмма нижней челюсти в боковой проекции 4.компьютерная томограмма Лечение Существует два метода лечения одонтогенных кист: 1. Цистотомия — удаление части стенки кисты и создание условий для длительного сообщения ( с полостью рта, полостью носа, верхнечелюстной пазухой), устраняющего основной механизм роста кисты- это повышение гидростатического давления. Показания к проведению цистотомии: -киста, в полость которой проецируется 3 и более интактных зубов, на рентгенограмме у корней последних не определяется периодонтальная щель -сопутствующие заболевания -большие кисты верхней челюсти с разрушением костного дна полости носа и небной пластинки -обширные кисты нижней челюсти с резким истончением основания челюсти ( толщиной кости менее 1-0,5 см) 2. Цистэктомия- удаление всей оболочки кисты костной полости Показания к проведению цистэктомии : -киста, как следствие порока развития одонтогенного эпителия -киста небольших размеров, расположенная в пределах 1-2 интактных зубов -обширная киста, при которых отсутствуют зубы в ее зоне и сохранен достаточный объем костной ткани ( для верхней челюсти — кисты, прилегающие или оттесняющие верхнечелюстную пазуху без явлений воспаления в пазухе) Причинные зубы при цистэктомии либо удаляются, либо сохраняются. При этом до оперативного вмешательства корневой канал герметично пломбируют, после чего проводится операция как правило с резекцией верхушки корня.
Данные методики лечения одонтогенных кист являются эффективными, однако необходимо помнить, что болезнь легче предупредить, чем лечить!
Лучшей профилактикой заболеваний являются ежегодное посещение врача-стоматолога для профилактического осмотра и периодическое рентгенологическое наблюдение ранее леченых зубов.
Множественные кисты челюстей: синдром Горлин-Гольца
Синдром Горлин-Гольца, также известный как синдром невоидной базальноклеточной карциномы (Nevoid Basal Cell Carcinoma Syndrome — NBCCS), является полисистемным нарушением, впервые описанным Горлином и Гольцом. Частота встречаемости этого заболевания оценивается в соотношении 1 случай на 50000-150000 человек и зависит от конкретного региона. Данное редкое аутосомно-доминантное заболевание характеризуется нарушением деятельности нескольких органов и систем, при котором поражаются скелет, глаза, кожа, репродуктивная и нервная системы. При этом все вышеперечисленные признаки редко наблюдаются одновременно у одного пациента. Патогенез синдрома связан с нарушением длинного плеча 9 хромосомы (q22.3-Q31) pTCH1-гена, клинические симптомы которого не проявляются при гетерогенном соотношении. Основные клинические признаки проявляются в форме множественных одонтогенных кератокист, базальноклеточных невусов и скелетных аномалий. В данной статье представлен случай заболевания у 16-летнего пациента, который обратился за помощью по поводу множественных одонтогенных кератокист, что впоследствии было диагностировано как синдром Горлин-Гольца. Подобный пример подчеркивает необходимость и важность тщательного клинического и рентгенографического обследования пациентов с кистами челюстей.
Клинический случай
16-летний пациент обратился на кафедру Челюстной медицины и радиологии Института стоматологических наук в Белгауме с главной жалобой на припухлость левой задней области нижней челюсти на протяжении последних 15 дней. Оказалось, что припухлость возникла внезапно, без сопутствующих приступов боли или каких-либо выделений. В истории болезни пациента, семейном анамнезе и имеющихся стоматологических данных не было обнаружено никаких фактов, которые могли бы спровоцировать или быть связаными с данной патологией. При общесоматическом обследовании было установлено, что пациент среднего телосложения, нормально упитан, с нормальной походкой, также был диагностирован кифоз. При внеротовом обследовании обнаружено асимметрию лица, прогнатию нижней челюсти, гипертелоризм и косоглазие левого глаза (фото 1). В ходе внутриротового осмотра обнаружена припухлость размером 3 см × 1 см, занимающая вестибулярную область от 34 до 36 зуба (33 зуб отсутствует). При пальпации припухлость твердой консистенции, безболезненна, расширяет щечную кортикальную пластинку в области 34-36 зубов. Основываясь на данных анамнеза и клинической картине, был поставлен предварительный диагноз одонтогенной кисты, с необходимостью проведения дифференциальной диагностики с одонтогенной кератокистой. На панорамной рентгенограмме были обнаружены четыре многоячеистые области рентгенопрозрачности и одно однокамерное просветление с зубчатыми краями. Области многоячеистых дефектов охватывали тело нижней челюсти, распространяясь вправо и влево к ветви челюсти и левому суставу. Однокамерная область просветления находилась в районе бугристости верхней челюсти слева (фото 3). Тонкоигольную аспирационную биопсию области припухлости проводили с использованием иглы 24 размера. Аспирированный состав имел кремово-белую окраску с концентрацией белка 3,3г/100 мл. Учитывая возможность проявления синдрома Горлин-Гольца, пациенту также сделали рентгенографию грудной клетки, компьютерную томографию (КТ) и боковую цефалографию. На рентгенограмме грудной клетки обнаружено расщепление 2, 3 и 4 ребер справа, и аналогичная картина 3-го и 4-го ребер слева (фото 4). На КТ диагностировано двустороннее расширяющееся литическое поражение нижней челюсти (фото 5), а на боковой цефалограмме – перекрытие турецкого седла (фото 6).
Фото 1. В ходе внеротового обследования обнаружена асимметрия, гипертелоризм и косоглазие.
Фото 2. Внутриротовая припухлость в области щечного преддверья ротовой полости.
Фото 3. На ортопантомограмме обнаружено несколько многоячеистых просветлений с зубчатыми краями.
Фото 4. Расщепление ребер на рентгенограмме грудной клетки.
Фото 5. Компьютерная томография диагностировала двустороннее расширяющееся литическое поражение нижней челюсти.
Фото 6. На боковой цефалограмме визуализируется перекрытие турецкого седла.
После проведение инцизивной биопсии в ходе гистопатологического исследования образца был обнаружен кистозный эпителий, состоящий из темно окрашенных базальных клеток, расположенных в виде палисадного узора. В поверхностном слое обнаружены явления паракератоза и гофрированный внешний вид, которые могли подтверждать диагноз кератокисты (фото 7).
Фото 7. Гиперхроматическкий палисадоподобный базальный слой и гофрированная паракератозная поверхность (гематоксилин-эозин, × 10).
Обсуждение
Синдром Горлин-Гольца возникает с одинаковой частотой как у мужчин, так и у женщин почти всех этнических груп. Заболевание диагностируется у молодых пациентов, в большинстве случаев – у людей в возрасте от 17 до 35 лет. Подобное патологическое состояние очень трудно диагностировать в раннем детстве, поскольку его симптомы проявляются постепенно в течение роста, но хороший прогноз лечения характерен в первую очередь для случаев, диагностированных на ранних стадиях. Основные и второстепенные симптомы данной патологии, обобщенные Evans и коллегами в 1993 году, помогут диагностировать синдром Горлин-Гольца.
Основные критерии:
- больше двух базальноклеточных карцином или одна у пациентов моложе 20 лет;
- одонтогенные кератокисты челюстей;
- три или больше ладонных или подошвенных углублений;
- двухслойные области кальцификации серпа мозга и мозжечка;
- расщепление, слияние или заметное выступание ребер;
- прямые родственники с присущим синдромом Горлин-Гольца.
Второстепенные критерии:
- макроцефалия;
- врожденные аномалии (расщелина губы или неба, выступающие лобные бугры, большое лицо, гипертелоризм умеренной или тяжелой степени);
- другие скелетные аномалии (деформации Шпренгеля, обширные деформации грудной клетки, синдактилия пальцев);
- рентгенологические аномалии, такие как перекрывание турецкого седла, аномалии позвоночника, дефекты рук и ног или огнеподобная форма очагов просветлений на руках и ногах;
- фиброма яичников или миелобластома.
Двух основных критериев или одного основного и двух второстепенных является достаточно для постановки диагноза синдрома Горлин-Гольца. В нашем случае диагноз был подтвержден наличием двух основных критериев (одонтогенные кератокситы челюстей и расщепление ребер) и двух второстепенных (врожденные аномалии: выступающие лобные бугры и гипертелоризмом; рентгенологические аномалии: кифоз и перекрытие турецкого седла).
Одонтогенные кератокисты могут быть первым симптомом синдрома. Их обычно обнаруживают случайно на рентгенологическом снимке. Кисты могут проявляться клинически в случае инфицирования в форме припухлости. В нашем случае диагностированные кисты были первым симптомом верифицированного позже синдрома. Одонтогенные кератокисты при синдроме Горлин-Гольца, как правило, представлены в форме однокамерных или многокамерных областей рентгенопрозрачности тела, угла или ветви челюсти.
Были предложены различные консервативные подходы к лечению больших кист у молодых пациентов, направленные на сохранение мягких и твердых тканей, в том числе и зубов. Они включают в себя приемы марсупиализации, декомпрессии, энуклеацию раствором Карнуа, периферическую остеоэктомию с или без использования раствора Карнуа, резекцию челюсти или хирургическое удаление кератокисты с последующей криотерапией раствором Карнуа. Генетическая консультация является обязательным мероприятием для всех пациентов, поскольку 50% пациентов могут передать заболевание ребенку. Пренатальную диагностику при беременности можно проводить в случаях выявленных мутаций в семье с синдромом в анамнезе.
В нашем случае пациент был направлен в отделение челюстно-лицевой хирургии, где ему провели энуклеацию и кюретаж кистозных поражений (фото 8). Пациент был проинформирован об особенностях синдрома с рекомендациями избегать длительного воздействия солнечных лучей. Через шесть месяцев на рентгенограмме обнаружено хороший прогресс заживления кистозных полостей с образованием костной ткани. Пациент до сих пор находится под наблюдением (фото 9).
Фото 8. Вид после хирургической энуклеации кисты.
Фото 9. Визуализация процесса заживление кости через 6 месяцев после операции.
Выводы
Пациенты с синдромом Горлин-Гольца требуют особого междисциплинарного медицинского и стоматологического подхода во время лечения. Ранняя диагностика обеспечивает профилактику осложнений и выбор правильного алгоритма лечения. Молодые пациенты без имеющейся базальноклеточной карциномы в анамнезе могут просто учитывать меры предосторожности и избегать радиационного облучения. Диагностированные и пролеченные пациенты должны находиться под строгим наблюдением, поскольку частота рецидивов синдрома достигает 63%.
Авторы: S. Manjima, Zameera Naik, Vaishali Keluskar, Anjana Bagewadi
Лечение кератокист челюстей с применением деминерализованного костного матрикса в сочетании с богатой тромбоцитами плазмой крови
Международная гистологическая классификации опухолей (МГКО) ВОЗ № 5 (1971) среди одонтогенных кист челюстей выделяла первичную кисту — кератокисту, которая является пороком развития зубообразовательного эпителия и развивается в зубосодержащих участках челюстей. В последней гистологической классификации одонтогенных опухолей ВОЗ (2005) — Pathology and Genetics, Head and Neck Tumours — кератокисты отнесены к опухолям и называются «доброкачественная кератокистоз- ная одонтогенная опухоль». Она имеет невосполи- тельное происхождение и является пороком развития остаточных элементов зубной пластинки [10,13]. Развиваются кератокисты в зубосодержащих участках челюстей: на верхней челюсти чаще встречается во фронтальном отделе, особенно в области клыков, а на нижней челюсти — в задней ее части или позади третьего моляра нижней челюсти с распространением на ветвь [1,15]. Одонтогенные кератокистозн- ные опухоли (ОКО) челюстных костей составляют, по данным разных авторов, от 5,4 до 17,4% от всех одонтогенных кист [6,11]. В некоторых случаях кера- токисты включаются в симптомокомплекс при врожденной патологии (синдром Горлина, синдром Мар- фана и др.). Они могут имитировать другие поражения, затрудняя диагностику, основанную только на клинико-рентгенологическом обследовании [3]. Рентгенологически одонтогенные кератокисты могут быть однокамерными или многокамерными [8].
Одонтогенная кератокиста вызывает большой интерес, главным образом, из-за тенденции к реци- дивированию [5,16]. По данным литературы процент рецидивов варьирует от 0 до 62.5% в зависимости от выбранной методики хирургического лечения [14,19]. После цистотомии этот показатель может со-ставить 40% [18], после цистэктомии -17.79-54.5% [14], тогда как после энуклеации с периферической остэктомией и блоковой резекции челюсти состав-ляет от 0-2% [14,18,19]. Разные авторы, видят разные причины рецидивирования. По мнению одних [8], возможным объяснением рецидивов является агрессивность кисты, обусловленная активностью коллагеназы в стенке кисты и высокой фибриноли- тической активностью. Другие авторы уделяют осо-бое внимание инфильтрации мягких тканей, прорастании в надкостницу, пролиферации эпителиальной выстелки [2,13], остаточным элементам зубной пластинки, которые могут формировать новые кисты, вид кератинизации (паракератинизированные кисты более агрессивны и склонны к рецидивам) [7,12,17].
Для лечения кератокист были предложенны разнообразные методы операций. .Т.Буге и J.Zakrzewska [7], рассмотрев методы лечения, описанные различными авторами, предложили их классификацию: 1. цистэктомия: с первичным закрытием, с заполнением участка дефекта, с химической обработкой, с криодеструкцией; 2. цистотомия: изолированно, двухэ-тапно с последующей цистэктомией; 3. резекция че-люсти. Р.Бгаш1еу [4] разработал показания к различным методам операции: мелкие однокамерные кисты должны удаляться целиком из внутриротового досту-па; при крупных кистах в труднодоступных участках рекомендована декомпрессия посредством цистотомии с вторичной цистэктомией; крупные многока-мерные кисты предложено лечить методом резекции с первичной костной пластикой.
За период 2003-2009 гг. под нашим наблюдением находились 16 больных с 16 одонтогенными ке- ратоцистическими опухолями (ОКО). Возраст больных колебался от 16 до 62 лет. Из общего числа па-циентов 10 (62.5%) мужчины и 6 (37.5%) женщины. Соотношение мужчин к женщинам составило 1.67:1. Из всех 16 ОКО 15 (93.75%) наблюдались на нижней челюсти и 1 (6.25%) на верхней. Из 15 пациентов с ОКО нижней челюсти у 10 они локализовались в об-ласти угла и ветви, у 4-х в области моляров и у 2-х в подбородочном отделе. У одной пациентки ОКО рас-полагалась на верхней челюсти интеррадикулярно, между 23 и 24 зубами.
Киста чаще обнаруживалась случайно — у 9 больных при рентгенологическом исследовании по поводу других заболеваниий челюстно-лицевой области, двое больных были направлены лечащим стоматологом с ошибочным диагнозом “фолликулярная киста в области угла нижней челюсти с ретенированным зу-бом «мудрости»”, 4 обратились с жалобами на асим-метрию лица в связи с незначительным выбуханием кортикальной пластинки нижней челюсти и одна пациентка обратилась с жалобами на безболезненную припухлость десны, размерами около 1см в диаметре, в области верхней челюсти слева. Рентгеноло-гическая картина заболевания характеризовалась на-личием кистовидного образования, чаще обширного, с четкими, нередко полициклическими контурами, многокамерного. На рентгенограммах определялась периодонтальная щель корней зубов, проецирующихся на область кисты. Несмотря на обширное внутрикостное поражение, выраженной деформации челюсти не отмечалось, что объясняется распро-странением процесса по длиннику кости в виде еди-ной полости. Диагноз ОКО базировался на клинико-рентгенологических данных и подтверждался патогистологическим исследованием операционного материала.
Рис.1. Ортопантомограмма пациента С. до лечения
У 9 больных с обширными кератокистами ниж-ней челюсти операция проводилась под общим эндо- трахеальным обезболиванием, а у 7, с мелкими кистами до 2-Зсм, под местным обезболиванием в амбулаторных условиях. У 9 больных с обширными ке- ратокистами, с прорастанием в окружающие мягкие ткани, была проведена сегментарная резекция нижней челюсти без нарушения непрерывности кости отступая на 1см от краев кистозного поражения. Макроскопически при вскрытии ОКО обнаруживалась единая полость, выполненная серовато-грязной кератиновой массой, являющейся продуктом слущивания и жизнедеятельности ороговевающегося эпи-телия оболочки кисты. Образовавшийся дефект ко-сти ва всех случаях восстанавливался одномоментно ДКМ-ом в виде блоков и в размельченном виде в сочетании с БоТП. Для профилактики перелома кости у этих больных осуществляли шинирование зубов с межчелюстной фиксацией. Больным с мелкими ки-стами проводилась цистэктомия с обязательной периферической остеоэктомией, во избежание реци-дивов. Оболочка кисты была тонкой и легко разрывалась при вылущивании. При прорастании ОКО в мягкие ткани проводилось их иссечение. В двух случаях, помимо применения костно-пластического материала, использовали мембрану из пчелиного воска в целях направленной регенерации тканей. Мор-фологическое исследование проведено у всех больных. Оболочка ОКО была представленна волокнистой соединительной тканью с преобладанием коллагеновых волокон и выстлана многослойным эпите-лием. В многослойном эпителии наблюдались явления кератинизации по типу паракератоза и ортокератоза. Постоперационный период у 14 больных протекал гладко, без осложнений. У 1 больного наблюдалось нагноение костной раны с расхождением швов. После проведенной адекватной консервативной терапии удалось купировать воспалительный процесс. Отдаленные постоперационные наблюдения от 3 до 9 лет не показали рецидивов ни в одном случае. Во всех случаях дефект кости был восстановлен с образованием органотипичной кости в сроках от 3 до 12 мес. в зависимости от размеров последнего.
Для примера приводим клинический случай
Рис.2. Ортопантомограмма пациента через два года после операции.
Пациент С. 49л. поступил в отделение челюстно-лицевой хирургии мед. 30.03.2009г. с жалобами на онемение нижней губы и подбородка справа в течение последних 3-4 мес. Обращался к стоматологу по поводу плановой санации полости рта, и на ортопантомограмме, сделанной в стом. клинике, были обнаружены ки-стозные образования в области тела и ветви нижней челюсти. Пациент был направлен на стационарное обследование и лечение. При внешнем осмотре асимметрии лица не отмечалось. Кожные покровы в цвете не изменены, открывание рта свободное. Со стороны полости рта видимых патологических изменений не наблюдалось. На ортопантомограмме визуализировалось просветление в области угла и ветви нижней челюсти с четкими полицикличными контурами, окруженная склеротическим ободком. Неоднородность оттенков просветления создавало картину многокамерности кистозного образования. С левой стороны в области тела нижней челюсти прослеживалось кистозное образование с более четкими контурами, округлой формы и однородностью. Размеры кистозной полости справа около 7×5 см, слева около 4.5 см в диаметре (рис. 1).
Операция проведена 2.04.09г. под общим эндо- трахеальным обезболиванием наружным доступом. Произведен дугообразный разрез в области угла и тела нижней челюсти справа на 2.5 см ниже нижнего края длиной 6-6.5 см. (рис.За). Мягкие ткани рас-сечены послойно до кости. После отсепаровки надкостницы виднелась бугристая, слегка вздутая наружная кортикальная пластинка ветви нижней че-люсти (рис.Зб). Под охлаждением физиологического раствора высверлили и удалили наружуню корти-кальную пластинку (рис.Зв). Макроскопически по-лость кисты была заполнена серовато-грязной кератиновой массой (рис.Зг). После тщательного вылущивания кисты была проведена резекция нижней челюсти отступая на 0.5-1 см от границ опухоли, сохраняя непрерывность нижней челюсти в области его заднего края (рис. Зд). Образовавшийся дефект был заполнен размельченным аллогенным ДКМ в комбинации с БоТП и поверх закрыт и изолирован от окружающих мягких тканей мембраной из пчелиного воска в целях направленной регенерации кости (рис. Зе,ж,з). Со стороны полости рта был удален
Рис.3. Этапы операции: а)маркирована линия разреза, б) обнажена наружная поверхность кости, в) высверливание кортикальной пластинки г) видна оболочка кератокисты, д) проведена резекция нижней челюсти, е) заполнение дефекта размельченным ДКМ с БоТП, ж,з)наложение мембраны из пчелиного воска поверх костно-пластического материала, и)ранаушита послойно с оставлением резинового выпускника, к) обнажено тело нижней челюсти слева, л) кистозная полость заполнена ДКМ с БоТП, м) наложена восковая мембрана.
46 периодонтитный зуб. Рану послойно ушили с оставлением резинового выпускника (рис.Зи). Аналогичным образом проведена операция с левой стороны внеротовым доступом с одной лишь разницей, что при удалении наружней кортикальной пластинки была выявлена оболочка радикулярной кисты с ки-стозным содержимым. Была проведена цистэкто- мия с апекэктомией 35 зуба. Остаточную костную полость заполнили аллогенным ДКМ с БоТП и изо-лировали от надкостницы мембраной из пчелиного воска (рис.3 к,л,м).
Через два года (рис.2, 4) после операции больной жалоб не предъявлял. Внешне асимметрии лица не наблюдалось. На ортопантомограмме наблюдалось восстановление костной ткани в области дефекта, хотя в центральных отделах дефекта плотность новообразованной кости уступала материнской.
Рис. 4 Внешний вид больного через два года после операции
Таким образом, полученные нами данные совпадают с литературными, свидетельствующими об отсутствии рецидивов при хирургическом лечении с резекцией челюстной кости, либо цистэктомией с периферической остеоэктомией. Несмотря на травма- тичность данного метода вмешательства, с возможностью интраоперационных повреждений анатомических структур (повреждение нервов, перелом ко-сти), на сегодняшний день он является самым надежным в плане профилактики рецидивов и озлокачествления, о чем свидетельствуют также ряд авторов [2,7,19, 20]. А восстановление образовавшегося дефекта аллогенным либо ксеногенным ДКМ, в сочетании с БоТП, способствует быстрому заживлению раны, ускорению процессов репаративной регенера-ции костной ткани, что укорачивает период постоперационной реабилитации больных.
Список литературы
- Губайдулина Е.Я., Цегельник Л.Н., Башилова Р.А., Комнова З.Д. Одонтогенная первичная киста (керато- киста) челюстей. Стоматология. 1986; №1: с.41-45.
- Черниговская В.Н. Кератокисты челюстных костей у детей. Авт. канд.мед.наук. М., 2009.18с.
- Ali M, Baughman RA. Maxillary odontogenic keratocyst: a common and serious clinical misdiagnosis. J Am Dent Assoc. 2003;134(7):877-83.
- Bramley P.A. The odontogenic keratocyst: an approach to treatmentlnt. J Oral Surg 1974;3:337-41.
- Brannon RB. The odontogenic keratocyst. Part I. Oral Surg Oral Med Oral Pathol. 1976;42:54-72.
- Cawson R.A., Binhie W.H., Speight P.M., Barrett A.W., Weight J.M. Lucas s pathology of tumors of the oral tissues. 5th ed. London Churchill Livingstone.1998, p. 25-44.
- Chemli H, Dhouib M, Karray F, Abdelmoula M. Risk factors for recurrence of maxillary odontogenic keratocysts. Rev Stomatol Chir Maxillofac. 2010 Sep;l 11(4): 189-92.
- Donath K. Cysts and tumors of the jaw bone. Verh Dtsch Ges Pathol. 1992;76:360-5.
- Eyre J.,.Zakrzewska Y.M. British J Oral Maxillofac Surg. 1985. vol.23, 3; p.195-203.
- Kramer IR, Pindborg J J, Shear M. The WHO histological typing of odontogenic tumours. Can- cer.1992;70(12):2988-94.
- Kreidler J., Raubenheimer E., van Heerden W. A retro spective analysis of 367 cystic lesions of the jaws the Ulm experience. J. Craniomaxillofac Surg. 1993.21:339-41.
- Lam KY, Chan AC. Odontogenic keratocyst: a clinico- pathologicalstudy in Hong Kong Chinese. Laryngoscope, 2000; 110:1328-32.
- Li TJ. The odontogenic keratocyst: a cyst, or a cystic neo-plasm? J Dent Res. 2011 Feb;90(2): 133-42.
- Morgan T.A., Burton C.C., Qian T. A retrospective review of treatment of the odontogenic keratocyst J Oral and Maxillofac Surg. 2005; vol.63(5): p.635-639.
- O’Neill R, Al-Hezaimi K. Identification of an odontogenic keratocyst and treatment with guided tissue regeneration. J Can Dent Assoc. 2011;77: b 6.
- Shear M. Developmental odontogenic cysts: an update. J Oral Pathol Med. 1994;23:1-11.
- Wright JM. The odontogenic keratocyst: orthokeratinized variant. Oral Surg. 1981;51:609-18.
- Zecha JA, Mendes RA, Lindeboom VB, van der Waal I. Recurrence rate of keratocystic odontogenic tumor after conservative surgical treatment without adjunctive thera-pies. Oral Oncol. 2010 Oct;46(10): 740-2.
- Zhao YF, Jin-Xiong W., Wang SP. Treatment of odonto-genic keratocysts. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2002;94:151-6.
- Zhou JL, Jiao SL, Chen XH, Wang YL Treatment of recur-rent odontogenic keratocyst with enucleation and cryosur-gery. Shanghai Kou Qiang Yi Xue. 2005Oct;14(5):476-8.