Препараты для местной анестезии (местные анестетики) – это лекарственные средства, которые вызывают потерю чувствительности нервных окончаний или блокируют передачу нервным импульсов по волокнам.
Важно не путать местную анестезию с общей (наркозом). При местной анестезии возникает потеря болевой, температурной и тактильной (на прикосновения) чувствительности, при этом эффект ограничен небольшим участком тела вокруг места введения препарата – местного анестетика. Кроме того, при местной анестезии пациент находится в сознании, в отличие от общей анестезии.
Виды анестезий
Различают три основных вида местной анестезии:
- Поверхностную (терминальную) – развивается на месте нанесения местного анестетика, чаще всего на слизистых оболочках – глаза, ротовой полости, желудка и т.д., а также на поверхности кожи;
- Проводниковую – развивается при введении местного анестетика в крупный нервный ствол, при этом теряется чувствительность в тех участках, за которые отвечает этот нерв (отдельным видом проводниковой анестезии является эпидуральная анестезия, когда раствор препарата вводят в пространство над твердой оболочкой спинного мозга – при этом теряется чувствительность в нижней части тела);
- Инфильтрационную – возникает при послойном пропитывании тканей тела человека раствором местного анестетика (самый распространенный вид местной анестезии).
Групповой особенностью препаратов для местной анестезии является обязательное наличие суффикса –КАИН в названии, благодаря чему можно сразу опознать местный анестетик среди других препаратов.
Тримекаин (Trimecainum)
Синонимы: 2,4,6 — триметилацетилат анилида диэтиламиноуксусной кислоты гидрохлорид. Тримекаин по фармакологическому действию близок к лидокаину. По анестезирующей активности в 2-3 раза превосходит новокаин, действует быстрее и длительнее, не раздражает тканей. Тримекаин несколько токсичнее новокаина, особенно в более высоких концентрациях. Препарат расширяет сосуды, в стоматологической практике применяется с вазоконстрикторами. Показания к применению • Инфильтрационное обезболивание вмешательств на верхней челюсти. • Проводниковая анестезия. • Поверхностная анестезия СОПР. Кроме того, тримекаин, как и лидокаин, может использоваться при желудочковых экстрасистолиях и тахиаритмии. Противопоказания Противопоказаниями являются гиперчувствительность к тримекаину, слабость синусового узла, AV блокада, выраженная брадикардия, кардиогенный шок, патология печени и почек. Способ применения Применяется преимущественно для проводникового и инфильтрационного обезболивания, реже — для поверхностной анестезии. Используется для инъекций в виде 2 % раствора, местно — в виде 3-5 % мази. Для замедления всасывания к раствору тримекаина добавляют адреналин (0,1 % раствор 1-2 капли на 5-10 мл раствора тримекаина). Максимальная общая доза для инъекционного введения составляет 300 мг. Взаимодействие с другими лекарственными средствами Вазоконстрикторы усиливают и удлиняют эффект тримекаина. Предварительное введение транквилизаторов и снотворных повышает эффект тримекаина.
Показания к применению
Препараты местных анестетиков широко используют в стоматологии для инфильтрационной анестезии – при экстракции (удалении) зуба, мелких операциях на пародонте (деснах).
С целью достижения поверхностной анестезии местные анестетики используют в офтальмологии – в виде глазных капель при операциях на конъюнктиве (при лазерной коррекции зрения, извлечения инородных тел из глаза) и роговице глаза.
Кроме того, местные анестетики для поверхностной анестезии используют при ранах, мелких хирургических операциях на коже и слизистых оболочках, при язвах, в том числе язвенной болезни желудка – некоторые препараты местных анестетиков (например, бензокаин) входят в состав комбинированных препаратов, снижающих кислотность желудочного сока (антациды).
Отдельные препараты (лидокаин) применяют при эндоскопической диагностике для облегчения проведения процедуры – обезболивания глотки перед введением трубки через рот или нос; постановки мочевого катетера.
Для достижения проводниковой анестезии местные анестетики используют при обезболивании родов (эпидуральная анестезия), операциях на органах малого таза и на нижних конечностях.
Местный анестетик лидокаин помимо местноанестезирующего действия оказывает антиаритмический эффект, поэтому его используют также при нарушениях сердечного ритма – аритмиях.
Добавки к анестетикам:
1) Вазоконстрикторы
Вазоконстрикторы – добавляются для повышения эффективности местной анестезии, а также для замедления поступления анестетиков в ток крови.
Адреналин
Адреналин применяется чаще всего. Относительно безопасным разведением адреналина является концентрация 1:200000, которая может быть обеспечена только в карпулированных препаратах.
Норадреналин
В качестве вазоконстриктора норадреналин применяется реже. Норадреналин, в отличие от адреналина, менее опасен у пациентов с сердечной патологией (ишемической болезнью сердца), но выше риск развития гипертонического криза при сопутствующей гипертонической болезни.
Применяют вместо адреналина при тиреотоксикозе и сахарном диабете. Противопоказан при глаукоме.
Филипрессин (октапрессин)
Филипрессин – синтетический препарат, не оказывающий прямого действия на сердце. Эффект связан с прямым действием его на гладкую мускулатуру сосудов. Противопоказан при беременности, т.к. может вызвать сокращения миометрия.
Нежелательные системные воздействия вазоконстрикторов:
- подъем артериального давления,
- тахикардия,
- нарушения ритма сердца,
- приступы стенокардии,
- централизация кровообращения,
- головная боль.
Группа риска при использовании вазоконстрикторов
: пациенты с глаукомой, тиреотоксикозом, сахарным диабетом; больные, принимающие препараты раувольфин, тиреоидные гормоны, трициклические антидепрессанты, антидепрессанты – ингибиторы МАО.
2) Консерванты
Парабены
(метилпарабен
–
метил-4-гидрооксибензонат, этилпарабен)
В качестве консервантов применяются эфиры парагидроксибензойной кислоты (парабены), которые обладают антибактериальным и противогрибковым действием.
Надо помнить, что парабены входят в состав различных косметических препаратов, кремов, зубных паст и могут провоцировать контактный дерматит, поэтому существует реальная опасность аллергии к местноанестезирующему препарату.
Парааминобензойная кислота (ПАБК), которая является метаболитом новокаина, имеет похожее строение с парабенами, что может вызвать перекрестные аллергические реакции. Многие лекарственные препараты (сульфаниламиды, пероральные антидиабетические, фуросемид и др.) являются производными ПАБК. Поэтому нецелесообразно использование препаратов, содержащих парабен, использовать при лекарственной аллергии на перечисленные медикаменты.
Наличие или отсутствие парабенов в местноанестезирующем препарате указывается производителем. Парабены могут вызывать сенсибилизацию организма, анафилактический шок.
3) Стабилизаторы
Сульфиты
(дисульфит натрия или калия) применяются в качестве стабилизаторов вазоконстрикторов. Аллергия к сульфитам наиболее часто встречается у пациентов с бронхиальной астмой (частота – около 5%), поэтому при лечении таких пациентов следует быть особенно осторожным. Сульфиты вызывают отеки, крапивницы, бронхоспазм через ирритантные рецепторы, нервные и вагусные рефлексы.
Классификация препаратов местных анестетиков
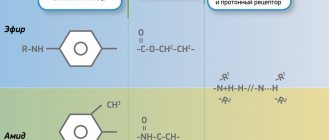
Местные анестетики классифицируют по клиническому применению (в зависимости от вида вызываемой анестезии), а также по химическому строению:
- Средства, которые используют только для поверхностной анестезии: сложные эфиры парааминобензойной кислоты: бензокаин, тетракаин;
- замещенные амиды ацетанилида: бумекаин, прилокаин.
- сложные эфиры парааминобензойной кислоты: прокаин;
- замещенные амиды ацетанилида: лидокаин.
Артикаин (Articainum)
Синонимы: ультракаин, убистезин, артикаин ИНИБСА, альфакаин, брилокаин, септонест. Метиловый эфир 4-метил-3-[2- пропиламнопропионамидо]-2-тиофенкарбоновой кислоты. Первый местный анестетик группы амидов, имеющий вместо бензольного кольца тиофеновое и дополнительную эфирную группу, синтезирован в 1969 г. Х. Рушинг с соавторами.
Препарат уступает лидокаину по жирорастворимости, что обусловливает меньшую возможность всасывания в кровь и поступления в ткани и органы. Для получения адекватной местной анестезии в стоматологии он используется в виде 4 % раствора. Артикаин обладает самым высоким соотношением активности и токсичности, т.е. имеет большую широту терапевтического действия, что делает его препаратом выбора у детей, лиц пожилого возраста и имеющих в анамнезе патологию печени и почек. По сравнению с другими амидными анестетиками имеет самый большой плазматический клиренс (3,9 л/мин) и самый короткий период полувыведения. Т1/2 артикаина составляет около 20 мин и зависит от содержания в растворе вазоконстриктора. Он не обнаруживается в грудном молоке в клинически значимых концентрациях, что свидетельствует о его преимуществах при выборе средств для местного обезболивания у кормящих матерей. Быстрота метаболизма и экскреции артикаина обусловливают отсутствие кумуляции при повторном его введении в ходе проведения большого объёма стоматологической помощи. Несмотря на короткий по сравнению с другими амидными местными анестетиками период полувыведения, высокий плазматический клиренс, препарат обладает средней длительностью действия. По сосудорасширяющей активности артикаин сходен с лидокаином, что обусловливает необходимость его применения с вазоконстрикторами. Высокая местноанестезирующая активность препарата позволяет уменьшить содержание в его растворе вазоконстриктора до 1:200 000. Низкая токсичность артикаина позволяет использовать его в 4 % растворе, имеющего высокую анестезирующую активность. Показания к применению • Инфильтрационное обезболивание вмешательств на верхней челюсти и в переднем отделе, включая премоляры, нижней челюсти.
• Проводниковая анестезия. • Интралигаментарная анестезия. • Внутрикостная анестезия. В обычно применяемых концентрациях артикаин не обладает поверхностноанестезирующим эффектом, но превосходит лидокаин, прилокаин и мепивакаин по активности при проведении инфильтрационной и проводниковой анестезии, позволяя приблизить эффективность местного обезболивания в стоматологии у взрослых к 95-100 %. У артикаина отмечается более высокая активность при воспалении в сравнении с другими анестетиками, используемыми в стоматологической практике. Поскольку артикаин в меньшей степени теряет свою активность при воспалении, он является препаратом выбора для обезболивания тканей при тяжёлых гнойно-воспалительных процессах. Предостережения В стоматологической практике перед введением местного анестетика рекомендуется проводить аспирационную пробу для профилактики внутрисосудистого введения препарата. Все растворы артикаина, содержащие вазоконстрикторы, следует с осторожностью назначать пациентам с сердечно-сосудистыми и эндокринными заболеваниями (тиреотоксикоз, сахарный диабет, пороки сердца, артериальная гипертензия и др.), а также получающим β-адреноблокаторы, трициклические антидепрессанты и ингибиторы МАО. При необходимости использования артикаина в период беременности, лактации, при сердечно-сосудистой недостаточности, сахарном диабете, тиреотоксикозе препаратом выбора является 4 % раствор артикаина с адреналином 1:200 000 или артикаин без вазоконстриктора. Побочные эффекты Побочные эффекты на препараты артикаина наблюдаются у 0,13-0,26 % пациентов. • Аллергические реакции (крапивница, ангионевротический отёк, анафилактический шок). • Отёк и воспаление в месте введения. • Умеренно выраженные нарушения гемодинамики и сердечного ритма, головная боль и тошнота.
• При случайном внутрисосудистом введении (особенно 4 % раствора артикаина с содержанием адреналина 1:100 000) возможна ишемия зоны введения, иногда прогрессирующая до некроза ткани. При использовании инфильтрационных методов введения препаратов артикаина с адреналином 1:100 000 изменения показателей гемодинамики у больных маловероятны. Для исключения повышения артериального давления и учащения частоты сердечных сокращений (пульса) при использовании проводникового обезболивания, что может быть связано с внутрисосудистым попаданием препарата, требуется обязательно проведение аспирационной пробы перед введением всей дозы препарата. Способ применения и дозы Препараты артикаина применяются для инфильтрационной и проводниковой анестезии. Для достижения полной анестезии при использовании 4 % раствор артикаина с адреналином 1:200 000 или 1:100 000 используется от 0,5 до 1,8 мл, в отдельных случаях может потребоваться дополнительное введение 1,0-1,8 мл. Уменьшение концентрации раствора артикаина до 2-3 % снижает эффект местного анестетика. Максимальная доза для взрослых — 7 мг/кг. Максимальная доза для детей — 5 мг/кг. Рекомендуется применять не более 1/2 максимально допустимой дозы.
Основы лечения местными анестетиками
Препараты для проводниковой и инфильтрационной анестезии выпускаются исключительно в виде растворов для инъекций, их относят к категории средств рецептурного отпуска. Введение этих препаратов осуществляется строго медицинским персоналом в условиях клиники и под обязательным контролем врача.
От момента введения местного анестетика до развития местной анестезии проходит от нескольких минут до получаса – все зависит от конкретного препарата. Поэтому нужно дождаться эффекта препарата и повторно его не вводить – это опасно ввиду развития токсического действия местного анестетика.
Продолжительность эффекта местных анестетиков различна и зависит от химического строения препарата: сложные эфиры парааминобензойной кислоты достаточно быстро разрушаются особыми ферментами-эстеразами в тканях человека, в то время как замещенные амиды ацетанилида к действию этих ферментов нечувствительны, потому оказывают гораздо более длительный местноанестезирующий эффект.
Типы местной анестезии
Тип и доза анестезии будут зависеть от многих факторов. Они включают в себя возраст пациентов, вес, аллергию, оперируемую часть тела и любое текущее состояние здоровья.
Различные препараты используются для блокирования боли. Их можно наносить в виде инъекций или путем нанесения спрея или мази.
Препарат действует, воздействуя на определенные нервные пути, чтобы нервы в области применения не посылали сигналы в мозг.
Как правило, препарат вступает в силу через несколько минут и проходит через несколько часов. Более сильная и более высокая доза будет длиться дольше.
Кокаин был первым анестетиком, но сейчас его используют редко. Лидокаин в настоящее время является наиболее широко используемым местным анестетиком, но для разных целей используются разные лекарства.
Для более длительных процедур бупивакаин является более подходящим, но он может быть более болезненным при первом применении. Следовательно, анестезиолог может сначала использовать лидокаин, а затем вводить бупивакаин, если онемение требуется на более длительный период.
Синтетические анестетики по своей структуре похожи на кокаин, но эти наркотики не обладают таким же потенциалом злоупотребления.
Особенности лечения местными анестетиками
Для проводниковой и инфильтрационной анестезии используют только стерильные растворы препаратов местных анестетиков.
Эффект местных анестетиков слабо проявляется или практически отсутствует при воспалении – в воспаленных тканях наблюдается повышенная кислотность (ацидоз), препятствующая поступлению препаратов местных анестетиков внутрь нервной клетки, что критически необходимо для развития эффекта лекарства.
Отдельные местные анестетики (артикаин, лидокаин) могут комбинировать с сосудосудивающими препаратами, в частности, с адреналином (эпинефрином). Это помогает местному анестетику дольше находиться в месте введения, не поступая в системный кровоток. При этом в несколько раз увеличивается длительность местноанестезирующего эффекта препарата. Кроме того, адреналин снижает токсичное действие местных анестетиков на организм.
Учитывая, что местные анестетики (особенно сложные эфиры) часто вызывают аллергические реакции, перед использованием этих препаратов желательно определить индивидуальную чувствительность к ним – ввести пациенту небольшое количество раствора местного анестетика под кожу предплечья и оценить реакцию через пять-десять минут.
Невозможно себе представить современную стоматологию без местной анестезии. Большинство терапевтических, некоторые ортопедические и практически все хирургические вмешательства проводятся после предварительного обезболивания. Широко используемые, заслуженно считающиеся наиболее эффективными и безопасными артикаинсодержащие местные анестетики позволяют при корректном соблюдении правил их применения избегать многих осложнений [3]. Но еще используют лидокаин и даже прокаин (новокаин), а в челюстно-лицевой хирургии — ропивакаин с целью длительного интра- и послеоперационного обезболивания, поэтому врачи должны хорошо понимать, насколько велик риск осложнений, непосредственно связанный с применением местных анестетиков (см. схему).
Остановимся на системных токсических реакциях на местные анестетики — одном из малоизученных осложнений, которое может привести к критическому исходу. В отличие от аллергических реакций системные токсические реакции на местные анестетики встречаются нередко, особенно при использовании высоких доз препаратов. За последние десятилетия учеными всего мира была проведена большая исследовательская и аналитическая работа по изучению токсического действия местных анестетиков на организм человека и определению ведущих признаков, отличающих это осложнение от аллергических реакций. Опубликованные результаты статистических исследований убедительно свидетельствуют о том, что современные местноанестезирующие препараты значительно менее опасны как аллергены (риск возникновения аллергии — 1:2 000 000 инъекций) и гораздо чаще вызывают системные токсические реакции (риск оценен как 1:1000 инъекций) [12].
Системные токсические реакции на местные анестетики в челюстно-лицевой хирургии и стоматологической практике, в отличие от общей хирургии, где эти препараты с целью региональной анестезии вводятся в значительно большем количестве, встречаются реже, но об этом осложнении необходимо помнить из-за вероятности их трагического исхода.
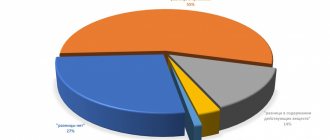
Современный рынок предоставляет стоматологам широкий выбор местных анестетиков. Важно при определении наиболее безопасного препарата ориентироваться прежде всего на его анестетический индекс, продолжительность эффективного действия и сочетаемость с другими препаратами, принимаемыми пациентом. В табл. 1 представлена информация о максимальных дозах, времени действия, активности и токсичности местных анестетиков.
Таблица 1. Анестезирующая активность, продолжительность действия, токсичность и максимально допустимая доза различных местных анестетиков Примечание. м/а — местный анестетик; м/а+в/к — местный анестетик с вазоконстриктором; активность — отношение минимальной действующей дозы новокаина к минимальной действующей дозе другого препарата; токсичность — отношение минимальной летальной дозы новокаина к минимальной летальной дозе другого препарата; анестетический индекс — отношение силы действия препарата к относительной токсичности препарата.
Обезболивающий эффект местного анестетика определяют его вазоактивность, жирорастворимость, способность связываться с протеинами и кислотность. Определенные коррективы, конечно, вносят соматический статус пациентов, а также происходящие в случае базисной лекарственной терапии фармакологические взаимодействия.
Скорость наступления анальгетического эффекта, системную абсорбцию, метаболизм и элиминацию местного анестетика определяют его физико-химические свойства. Так, жирорастворимость и протеинсвязывающая характеристики местного анестетика зависят от его тропности к клеточной оболочке нейрона, которая состоит из жира (90%) и протеина (10%). Чем выше жирорастворимость препарата, тем легче он проникает через оболочку, следовательно более эффективен. Чем лучше анестетик связывается с протеином, тем больше продолжительность его действия. Константа диссоциации препарата определяет скорость наступления анальгетического эффекта, а также абсорбции и элиминации.
После инъекции часть анестетика диффундирует на мембрану нейрона; оставшийся препарат попадает в сосудистое русло. Повышенная абсорбция местного анестетика приравнивается к прямому попаданию в сосуд; особенно этого следует опасаться в условиях кислой среды воспалительного очага. Количество абсорбированного сосудами препарата зависит от васкуляризации и величины кровотока в анестезированной ткани, а также влияния местного анестетика на тонус сосудистой стенки. При инфильтрационной анестезии амидные анестетики среднего и длительного действия вызывают вазодилатацию, а ропивакаин (наропин) в отличие от других длительно действующих препаратов (бупивакаин гидрохлорид — маркаин), дает сосудосуживающий эффект. Если в местноанестезирующем препарате содержится вазоконстриктор, скорость системной абсорбции замедляется, но появляется риск развития тахикардии и мерцательной аритмии.
До недавнего времени считалось, что степень проявления системной токсической реакции строго зависит от концентрации и количества вводимого анестетика. Так, на примере лидокаина (рис. 1) были показаны пиковые уровни концентрации анестетика в плазме крови, определяющие возможную клиническую картину системной токсической реакции.
Рис. 1. Зависимость клинических проявлений системной токсической реакции лидокаина от уровня его плазменной концентрации.
Однако, по данным публикаций последних лет, описанные случаи системной токсичности местных анестетиков в практике общей и челюстно-лицевой хирургии позволили предположить, что проявление токсических реакций не всегда зависит от излишнего количества введенного анестетика; даже рекомендуемые к применению дозы препаратов могут вызвать это осложнение [6, 16, 18].
Клинически системное токсическое действие местных анестетиков чаще проявляется симптомами повреждения ЦНС и реже — кардиоваскулярной. В связи с разнообразием условий, определяющих сроки и скорость поступления местноанестезирующего препарата в сосудистое русло, период развития клинической симптоматики системной токсичности колеблется в достаточно широких пределах — от 1—5 до >60 мин [10].
По тяжести клинических симптомов в системной токсичности местных анестетиков выделяют 3 степени [2]. При легкой ее степени (малые токсические реакции) первые жалобы пациента — на покалывание и зуд в области введения анестетика; эти ощущения могут распространяться на губы и язык. Одновременно появляются шум в ушах и металлический привкус во рту. Дыхание и гемодинамика не нарушены, может отмечаться умеренная тахикардия. Поскольку сознание пациента сохранено, изменения в самочувствии, как правило, не остаются незамеченными; они вызывают у пациента определенное беспокойство, нарастающее по мере усиления симптоматики; нередко присоединяется чувство страха. Клиническая картина развития токсической реакции может ограничиваться этим, постепенно неприятные ощущения проходят без дополнительных лечебных мероприятий, пациент успокаивается. Чаще всего легкие осложнения местной анестезии остаются не замеченными врачом и не фиксируются в истории болезни. Но если к субъективным ощущениям пациента присоединяются дрожь, подергивания отдельных мышц, тошнота, возможно, и рвота, отмечаются признаки нарушения сознания, в частности ориентации, следует понимать, что токсическая реакция развивается и переходит уже в среднюю степень тяжести. При максимальной выраженности клинических проявлений в этой стадии сознание пациента становится спутанным, речь нарушена, характерны оцепенение и заторможенность, отмечаются учащенное дыхание, снижение артериального давления, брадикардия, двигательное возбуждение или судороги. Появление судорог свидетельствует о том, что системная токсическая реакция переходит в тяжелую степень. На фоне судорог могут произойти потеря сознания, снижение мышечного тонуса, нарушение дыхания вплоть до апноэ, аритмии, асистолия, расслабление и паралич сфинктеров. Без оказания пациентам в критическом состоянии экстренной помощи, включающей в себя реанимационные мероприятия с обязательными специфическими элементами, неизбежен летальный исход.
Системная токсическая реакция на местные анестетики клинически не обязательно проявляется всеми перечисленными признаками, нередко наблюдаются отдельные из них. Анализ 93 случаев системной токсичности местных анестетиков показал, что классическая клиническая картина развивалась только у 60% пострадавших; преобладание патологических признаков со стороны ЦНС с кардиоваскулярными нарушениями наблюдается в 30,3% случаев, и только изолированные сердечно-сосудистые нарушения описаны у 9,7% пациентов [10].
Частота клинических признаков, свидетельствующих о развитии системной токсической реакции при случайном внутрисосудистом введении местного анестетика, представлена на рис. 2.
Рис. 2. Частота развития клинических признаков токсического действия местных анестетиков [7].
Из-за сложности проведения исследований (на человеке их выполнить невозможно!) до конца механизм развития системной токсичности остается непонятным. На сегодня известно, что местные анестетики тормозят процесс окислительного фосфорилирования, поэтому наиболее тяжелые нарушения происходят в органах, хуже всего приспособленных к анаэробному метаболизму дыхания, а это прежде всего головной мозг и сердце [2].
Считается, что токсическое влияние на клетки головного мозга определяет способность местного анестетика проникать через гематоэнцефалический барьер и блокировать натриевые каналы возбудимых клеточных мембран, что вызывает разные по тяжести токсические реакции. Если появляется судорожный синдром, сопровождающий его метаболический ацидоз повышает захват препарата не только нейронами головного мозга, но и кар-диомиоцитами.
Кардиотоксичность, вероятно, прежде всего определяется способностью местных анестетиков обратимо связываться с внутриклеточной частью потенциалзависимых натриевых каналов кардиомиоцита, препятствуя их открытию и тем самым предотвращая генерацию потенциала действия и его распространение вдоль нервного волокна. И чем выше эта способность анестетика, тем сильнее его обезболивающий эффект, но вместе с тем — и тормозящее влияние на проводящую систему сердца [8].
Все местные анестетики в высоких концентрациях увеличивают рефрактерный период сердца, угнетают возбудимость, сократимость и проводимость миокарда — значит, в превышающих допустимые концентрации дозах любой из местноанестезирующих препаратов может вызвать тяжелую депрессию миокарда. Важно отметить, что клиническая картина системной токсичности, вызванная лидокаином, проявляется прежде всего выраженными патологическими реакциями со стороны ЦНС; это позволяет врачу вовремя принять необходимые меры по спасению пациента. А более мощные по сравнению с лидокаином препараты даже в считающейся допустимой плазменной концентрации могут, не вызывая конвульсивных проявлений и не снижая сократительной способности миокарда, спровоцировать различные по тяжести аритмии [8].
Особая осторожность при проведении местной анестезии требуется пациентам с факторами риска по системной токсичности; к ним относят анемию; гипопротеинемию; хроническую сердечную недостаточность с застойными явлениями; нарушение функции печени и почек; эндокринные и обменные заболевания; беременность; пожилой возраст и ранний возраст (дети). По сравнению со взрослыми у детей раннего возраста значительно выше отношение сердечного выброса и регионарного кровотока к массе тела, и системные токсические реакции у детей развиваются быстрее в связи с быстрым нарастанием пиковых токсических концентраций препарата в плазме. Так, у ребенка 3 лет после аппликационной анестезии происходит почти мгновенная абсорбция местного анестетика, а время наступления пиковой плазменной концентрации лидокаина при проведении инфильтрационной анестезии сравнимо с таковым при его внутривенном введении.
Отдельно следует остановиться на лечении пациентов под седацией и общей анестезией с использованием местных анестетиков. В литературе [10] описаны 2 случая системной токсичности у младенцев 6 и 9 мес во время проведения уранопластики под общей анестезией через несколько минут после инфильтрации местного анестетика (в одном случае — лидокаина, в другом — артикаина). Проявившийся судорожный синдром не оставил сомнений в диагнозе, и помощь была оказана своевременно. По завершении послеоперационной реабилитации пациентов выписали из стационара без неврологического дефицита. Анализ других эпизодов системной токсичности, возникших во время общей анестезии, показывает, что чаще проявляются признаки осложнения со стороны сердечно-сосудистой системы, поскольку ЦНС блокирована, и ранние симптомы остаются незамеченными.
Профилактика токсического действия местных анестетиков
Системную токсическую реакцию можно предвидеть в случаях планируемого лечения пациентов группы риска, при превышении рекомендуемой дозы анестетиков, несоблюдении методики проведения анестезии. Но, к сожалению, не существует гарантирующего варианта предупреждения этого осложнения [15].
Профилактика системной токсичности заключается в строгом соблюдении инструкций по применению местных анестетиков, безошибочном выполнении техники анестезии и внимательном отношении к пациенту как на этапе подготовки к лечению, так и во время его проведения.
При первичной консультации обязательно выясняйте полную информацию о здоровье пациента. При наличии сопутствующих соматических заболеваний получите выписку из истории болезни с указанием диагноза и рекомендованной к применению базисной терапии. В случае необходимости проведите дополнительное обследование. Перед лечением обязательно определите физическое состояние больного и зафиксируйте в истории болезни основные параметры (цифры артериального давления, частоты сердечных сокращений, частоты дыхания). Обязательно проинформируйте пациента о возможных рисках и получите его письменное согласие на проведение всех запланированных вмешательств [3].
При выборе местноанестезирующего препарата обязательно предпочтите наименее токсичные из них, если это позволяет ситуация. Использование местных анестетиков длительного действия оправдано при длительных вмешательствах, требующих пролонгированного после-операционного обезболивания, и только при наличии полного набора реанимационного оборудования.
Обязательно используйте минимально эффективную дозу местного анестетика, выбирайте достаточную его концентрацию и не превышайте необходимый объем анестетика. Учитывайте абсорбционные способности окружающих тканей в месте проведения инъекции [4].
Перед введением анестетика обязательно проводите аспирационную пробу и повторяйте ее, если перемещаете иглу по ходу введения; не забывайте, что результаты аспирационной пробы бывают ложноотрицательными примерно в 2% случаев. Для повышения безопасности при возможности используйте ультразвуковую навигацию во время проведения инъекции, хотя ее эффективность еще мало изучена и риск внутрисосудистого введения анестетика остается [5].
Обязательно вводите местный анестетик постепенно, медленно (1 мл/мин) или дробно с паузами в 15—30 с. При введении больших порций анестетика интервал введения необходимо увеличивать для снижения кумуляции [4].
Не прерывайте вербальный контакт с пациентом во время проведения местной анестезии; обязательно наблюдайте за его реакцией во время манипуляции и активно выявляйте жалобы — это повышает вероятность того, что первые субъективные признаки развивающейся системной токсической реакции будут замечены вами вовремя [3].
Ниже представлены максимально допустимые дозы наиболее употребляемых в амбулаторной стоматологической практике местных анестетиков для детей и взрослых (табл. 2—5).
Таблица 2. Максимально допустимые дозы лидокаина 2%
Таблица 3. Максимально допустимые дозы мепивакаина 2%
Таблица 4. Максимально допустимые дозы артикаина 4%
Таблица 5. Максимально допустимые дозы мепивакаина 3%
Лечебные мероприятия при системной токсической реакции
До недавнего времени лечение системных токсических нарушений, вызванных местными анестетиками, предусматривало использование противосудорожных препаратов, обеспечение адекватной оксигенации пациента вплоть до интубации трахеи с последующим проведением искусственной вентиляции легких, инфузионную терапию большими объемами кровезаменителей с введением глюкокортикостероидов и препаратов, корригирующих кардиоваскулярные нарушения. Проведение при необходимости сердечно-легочно-церебральной реанимации не предусматривало никаких особенностей, комплекс выполнялся по общему протоколу [1].
В настоящее время наряду с мероприятиями по замещению витальных функций пациента приоритет в лечении системной токсичности принадлежит снижению, а по возможности — устранению системного действия местных анестетиков [13]. Рекомендованное внутривенное введение липидных растворов, эффективность которых доказана экспериментально и клинически [9], позволяет купировать симптомы токсичности за счет связывания липофильных местных анестетиков. Плазменная концентрация препаратов снижается, происходит их «вымывание» (отсоединение по градиенту концентрации от мембраны нейрона и кардиомиоцита) и выведение с новыми порциями липида. Кроме того, известно, что содержащие липиды растворы являются энергетическим субстратом для митохондрий сердца и эта их способность оказывается востребованной в случае кардиотоксических реакций. Лечебная схема с использованием для устранения системных токсических реакций местных анестетиков раствора интралипида (20%) была названа «липидным спасением» [7].
Клиническая картина тяжелой стадии системной токсичности местных анестетиков может развиваться стремительно, поэтому очень важно правильно оценить первые симптомы и вовремя приступить к оказанию экстренной помощи. Судорожный синдром по-прежнему является абсолютным показанием к применению бензодиазепинов; опаснее купировать его пропофолом или барбитуратами ультракороткого действия из-за их собственного выраженного кардиодепрессивного действия. Как и в прежних рекомендациях, одним из первых мер по спасению пациента является обеспечение его адекватной оксигенации любым доступным способом, включая интубацию трахеи и аппаратную искусственную вентиляцию легких 100% кислородом. В случае неэффективного кровообращения на фоне аритмии или асистолии незамедлительно следует приступить к проведению реанимационных мероприятий и продолжать их не менее 60 мин. Поскольку местные анестетики не вызывают необратимых изменений миокарда, при достаточной оксигенации головного мозга и введении липидных растворов в течение этого времени остается надежда на спасение пациента. Крайне важно не спешить прекращать эффективные реанимационные мероприятия, если системная токсичность вызвана мощными анестетиками, потому что на их «вымывание» требуется длительный период времени [6]. При проведении в случае необходимости симптоматической терапии нужно избегать введения липофильных препаратов — β-блокаторов и блокаторов кальциевых каналов, отказаться от вазопрессина, для купирования желудочковых аритмий использовать только амиодарон (кордарон), снизить дозировку эпинефрина (адреналина) до менее чем 0,1 мкг/кг или полностью отказаться от его введения [13].
Источники литературы [20] сообщают о том, что при системной токсической реакции на местные анестетики быстрое введение больших объемов липидных растворов не сопровождается значительными осложнениями, а их клиническая эффективность на фоне реанимационных мероприятий позволяет избежать остаточных кардиологических нарушений и неврологического дефицита [10, 17].
Для «липидного вымывания» можно использовать любую жировую эмульсию, но лучше всего себя зарекомендовал интралипид (20%) [11]. Не следует проводить инактивацию местных анестетиков диприваном (пропофолом) из-за необходимости для получения положительного результата большого количества препарата в связи с низким содержанием в нем липидов, а это опасно, поскольку диприван дает прямой кардиодепрессивный эффект [15]. Сегодня купирование системной токсической реакции на местные анестетики рекомендовано проводить липидами, начиная введение препарата при появлении первых характерных жалоб или симптомов и одновременно быть готовым к выполнению полного комплекса реанимационных мероприятий [6].
В каждом лечебном учреждении, в том числе стоматологическом, где используются местные анестетики, необходимо иметь 1 л раствора жировой эмульсии (интралипид 20% — 500 мл или иной), шприцы для проведения «липидного вымывания» объемом 50 мл, периферические внутривенные катетеры 14—16 G, системы для инфузии, копию протокола «липидное спасение» («LipidRescue») [19].
После катетеризации периферической вены начинать вводить липидный раствор необходимо болюсно (интралипид 20% — 1,5 мл/кг) при помощи шприцев 50 мл, затем перейти на капельную инфузию (интралипид 20%, скорость — 0,25 мл/кг/мин) и продолжать введение препарата в таком темпе не менее 10 минут уже после стабилизации кровообращения. Если этой дозой липидного раствора стабилизировать кровообращение не удается, необходимо повторить его болюсное введение в той же дозировке (интралипид 20% — 1,5 мл/кг) и перейти на ускоренную инфузию препарата (интралипид 20%, скорость — 0,5 мл/кг/мин). Допустима высшая разовая доза жировой эмульсии — 10 мл/кг/мин.
На форуме «Euroаnaesthesiа-2010» в Хельсинки (Финляндия) Европейским советом по анестезиологии (European Board of Anaesthesiology) совместно с Европейским обществом анестезиологии (European Society of Anaesthesiology) была принята декларация по безопасности пациентов в анестезиологии. В ней предусмотрены основополагающие моменты, позволяющие предупреждать и избегать серьезных осложнений, предотвращать опасность для пациентов. В частности, указано, что все лечебные учреждения, в которых используются местные анестетики «…должны иметь протоколы и средства, необходимые в ситуации системной токсичности…» [14]. Хельсинкская декларация была одобрена Всемирной организацией здравоохранения (World Health Organization), Всемирной федерацией обществ анестезиологов (World Federation of Societies of Anaesthesiologists) и Федерацией пациентов Европы (European Patients Federation). С учетом особенностей каждая страна вправе доработать и адаптировать к своим условиям протокол проведения реанимации с использованием липидных растворов. Мы считаем эту задачу крайне важной для нашего врачебного сообщества.
Авторы заявляют об отсутствии конфликта интересов.
Бумекаин
Синонимы: пиромекаин. Показания к применению
Пиромекаин применяется для поверхностной анестезии при стоматите, гингивите, глоссите, пульпите, для обезболивания места инъекции и снятия повышенного рвотного рефлекса. Способ применения и дозы Пиромекаин в стоматологии используется только для поверхностной анестезии: в виде 1 % раствора для подавления рвотного рефлекса при снятии слепков; 1-2 % раствор и 5 % пиромекаиновая мазь используются для обезболивания СОПР. Для стоматологической практики разработана мазь, содержащая 5 % пиромекаина и 5 % метилурацила, оказывающего противовоспалительное действие и стимулирующего процессы регенерации. При лечении воспалительных заболеваний полости рта мазь можно применять 1-3 раза в сутки. Доза мази не должна превышать 1 г.