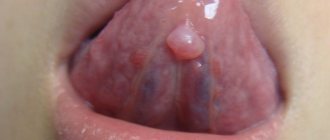
Сиаладеноз — это невоспалительное заболевание слюнных желез, приводящее к увеличению и/или нарушению их функции. Поражение носит дистрофический характер и не связано с появлением опухолей. Структурные изменения тканей желез обычно появляются на фоне других системных патологий. Стоматологи достаточно часто сталкиваются с таким явлением: 1 случай из 10 патологий слюнных желез представлен именно сиаладенозом.
Обычно заболевание возникает у людей среднего возраста. Поскольку оно часто сопровождает эндокринные, аллергические, дисметаболические и другие системные болезни, подход к лечению должен осуществляться не только со стоматологической стороны.
Виды сиаладенозов
По расположению патологических изменений выделяют следующие виды сиаладенозов:
- интерстициальный;
- паренхиматозный;
- протоковый.
Патологические участки могут располагаться как в тканях самой железы, так и в протоках.
По степени выраженности различают несколько стадий:
- Первая. Слюнные железы имеют обычные размеры и слабо пальпируются.
- Вторая. Наблюдается незначительное увеличение желез, которое незаметно при визуальном осмотре, но пальпируется.
- Третья. Увеличение желез, которое заметно и при визуальном осмотре, и прощупывании.
По природе происхождения выделяют нейрогенные, аллергические, эндокринные сиаладенозы, а также алиментарные — связанные с особенностями питания.
Задать вопрос
Материал и методы
В профильном отделении кафедры челюстно-лицевой хирургии (ЧЛХ) в Центре cтоматологии (ЦС) Московского государственного медико-стоматологического университета (МГМСУ) им. А.И. Евдокимова на обследовании и лечении находились 25 человек в возрасте от 25 до 50 лет с хроническим паренхиматозным сиалоаденитом. Критерием включения в исследование служило наличие хронического паренхиматозного сиалоаденита. Критерием невключения являлось наличие сопутствующей патологии в острой стадии или стадии обострения. Критерием исключения становился отказ пациентов от дальнейшего участия в исследованиях. Для постановки диагноза у всех пациентов проводилось клиническое обследование, которое включало осмотр и пальпацию измененной слюнной железы, установление ее размеров и количества выделяемого секрета, сбор анамнеза о сопутствующих заболеваниях.
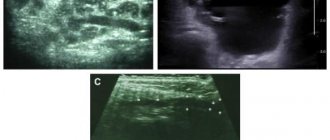
Также всем пациентам было проведено ультразвуковое исследование (УЗИ) высокого разрешения в В-режиме и режиме цветового допплеровского картирования на ультразвуковом сканере Philips iU-22 с применением датчиков линейного сканирования частотой 5—17 МГц. Дополнительно у пациентов в течение 5 мин осуществляли сбор смешанной слюны в стерильную пластиковую пробирку с плотно завинчивающейся крышкой. Образцы центрифугировали и в супернатанте слюны спектрофотометрическим методом определяли содержание белка альбумина (в мг/мл) и иммуноферментным методом количество иммуноглобулина (Ig) G. Исходные данные ультразвуковой допплерографии и смешанной слюны сопоставлялись с результатами исследования на 7-е сутки и через 1 мес от начала лечения пациентов.
По методу предлагаемого лечения пациенты были разделены на две группы. Пациентам 1-й группы (n
=11) проводили стандартную антибактериальную и спазмолитическую терапию
per os
в течение 5 дней следующими препаратами: усиленный амоксицилин 625 мг по 1 таблетке 3 раза в день, дротаверин по 1 таблетке 2 раза в день. Пациентам 2-й группы (
n
=14), наряду со стандартной терапией, назначали
per os
комплексную антигомотоксическую терапию препаратами траумель С по 1 грануле 3 раза в день и лимфомиозот по 15 капель 3 раза в день в течение 24 дней, спаскупрель по 1 таблетке 2 раза в день курсом на 5 дней. Все манипуляции осуществлялись только после информированного согласия пациента, подписанного им и лечащим врачом в двух экземплярах. Обоснованием для применения данных гомеопатических препаратов явилось то, что траумель С является высокоэффективным средством при воспалительных процессах, препарат спаскупрель оказывает спазмолитическое, обезболивающее, седативное и противосудорожное действие, препарат лимфомиозот улучшает микроциркуляцию периферических сосудов. Все полученные цифровые значения были обработаны методом вариационной статистики с использованием программы Statistica 8.0.
Почему возникает сиаладеноз
Сиалоз может развиваться на фоне основных заболеваний или быть вызван некоторыми физиологическими причинами. Например, патология встречается у женщин во время беременности и лактации. Патологические изменения нередко спровоцированы аутоиммунными недугами — системной склеродермией, ревматизмом, псориазом и пр., а также метаболическими и эндокринными расстройствами.
Среди нарушений питания, приводящих к сиалозу, относят строгие затяжные диеты и ограничения, анорексию. В целом самыми распространенными причинами выступает сахарный диабет, нарушения менструальной функции и работы щитовидной железы, хронические панкреатиты и иные патологии ЖКТ.
Аллергическая природа болезни может быть связана с лекарственной аллергией. В некоторых случаях сиалоз слюнных желез развивается после перенесенной операции или травмы в области зубочелюстной системы.
Причины развития сиаладенозов
Сиаладеноз может быть вызван как физиологическими причинами, так и патологическим состоянием пациента, а именно:
- беременностью;
- грудным вскармливанием;
- злоупотреблением алкоголем;
- нарушениями эндокринной системы;
- сахарным диабетом;
- нарушением менструального цикла (гиперменструальным синдромом);
- простатитом;
- хроническим панкреатитом;
- аутоиммунными заболеваниями (ревматоидным артритом, системной красной волчанкой, склеродермией, псориазом, болезнью Шегрена, болезнью Микулича и др.);
- пониженным питанием вследствие нервной анорексии.
Также у пациентов могут развиваться аллергические сиаладенозы при приеме некоторых лекарственных препаратов. Возможно возникновение сиаладеноза после хирургического вмешательства на слюнной железе или ее травмирования. Главной и наиболее распространенной причиной проявления сиаладенозов у пациентов, которые страдают от алкоголизма, является цирроз печени. Также нередки случаи развития сиаладенозов неясного происхождения у пациентов, которые не имеют каких-либо системных заболеваний. В данном случае больной проходит обследование с целью выявления общего заболевания. Сам по себе механизм развития этой патологии в медицинской практике до конца неясен. Но в медицине выделяют такие факторы проявления данного заболевания, как:
- нейропатия, которая сопровождается разрушением нервных волокон;
- нарушения в системе микроциркуляторного русла и окисления липидов, что приводит к повреждению тканей клеток;
- врожденное расширение и нарушение архитектоники протоковой системы.
Эти процессы вызывают функциональную недостаточность и замещение железистой ткани жировой.
Симптомы заболевания
Сиалозы чаще поражают околоушные, редко — поднижнечелюстные и подъязычные железы. Обычно речь идет о двустороннем патологическом процессе. Картина заболевания неспецифична — появляется болезненный отек в области пораженных желез, их увеличение на 2-й и 3-й стадии. Увеличение сохраняется в течение долгого времени.
Одним из проявлений болезни является сухость в полости рта. Это связано с тем, что слюноотделение при болезни может быть недостаточным.
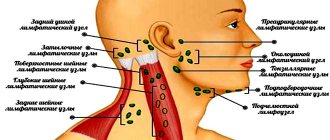
При осмотре врач определит характерную припухлость мягких тканей. Прощупывание не доставляет сильной боли, иногда появляются дискомфортные или слабо болезненные ощущения. Близко расположенные лимфатические узлы не изменены, а ограничений в открытии рта нет. Во время массажа слюнной железы выделяется прозрачная слюна без внешних особенностей.
Стоит отметить, что специфические симптомы могут сопровождать сиалозы, протекающие с пониженным или повышенным слюноотделением без увеличения самих желез. Например, такое наблюдается при стоматитах, язве двенадцатиперстной кишки, паразитозах, неврастении и пр.
Особенности диагностики
Обследование человека с подозрением на сиаладеноз может включать следующие методы:
- опрос, осмотр, прощупывание желез;
- лабораторные исследования — общий и биохимический анализы крови, клинические исследования мочи, оценка углеводного обмена (анализ на глюкозу);
- УЗИ слюнных желез и мягких тканей — необходимо для подтверждения невоспалительного характера болезни и исключения опухолей.
Врачу важно исключить другие возможные патологии, характеризующиеся увеличением слюнных желез: воспалительные заболевания, инфекционные болезни, кисты и опухоли, образование конкрементов (камней).
Сиалография назначается для определения расширенных или суженных слюнных протоков, она предусматривает введение контрастного препарата. Радиосиалограмма также может потребоваться для оценки секреторной способности желез. С помощью КТ врач может увидеть двухстороннее увеличение размеров и плотности тканей, исключить злокачественные и доброкачественные образования.
В качестве дополнительного метода могут быть задействованы сиалометрия, цитологические изучения секрета (слюнной жидкости), а также биохимическое исследование слюны. Окончательный диагноз может быть поставлен после аспирационной или иного вида биопсии желез. Гистологическое изучение позволяет установить дистрофические изменения.
Чтобы выяснить точную причину болезни, важно оценить общее состояние здоровья. Поэтому нередко пациент нуждается в осмотре другим специалистом узкого профиля: эндокринологом, гинекологом, урологом, аллергологом и пр. В ряде случаев требуется привлечение ревматолога.
Методы лечения
Лечение сиаладеноза — многоступенчатый процесс. Главным условием является эффективная терапия основного или сопутствующего заболевания, хотя это и не поможет решить проблему полностью. Симптоматическая терапия возможна с помощью новокаиновых блокад. Физиотерапия поможет справиться с неприятными симптомами, широко применяются электрофорез, гальванизация, магнито- и лазеротерапия. Воздействие осуществляется на область шейных нервных тканей с целью улучшения проводимости импульсов.
Медикаментозная терапия состоит в применении витамина Е, препаратов для стимуляции слюноотделения, а также коллоидных растворов для коррекции вязкости крови, улучшения кровотока в мелких кровеносных сосудах. Хирургическое лечение может быть показано при отсутствии положительного ответа на консервативную терапию. Оно заключается в частичном или полном удалении слюнной железы или ее протока.
Результаты и обсуждение
Как видно из данных табл. 1, при длительном течении СД-2 отмечали увеличение уровня ИЛ-2 и снижение ИФН-γ в РЖ. Уровень ИЛ-1β был наиболее высоким в группе больных с длительностью СД-2 ≤5 лет.
Таблица 1. Содержание цитокинов в РЖ у больных сиалозом и СД-2 различной длительности (M±m)
Table 1. Cytokine content in the oral fluid of patients with sialosis and type 2 diabetes (M±m)
| Показатель | Практически здоровые (n=10) | Все больные (n=40) | Длительность СД-2 | |
| ≤5 лет (n=15) | >5 лет (n=25) | |||
| ИЛ-1β, пг/мл | 42,3±3,7 | 45,3±1,0 | 46,7±1,5 | 44,5±1,4 |
| ИЛ-2, пг/мл | 11,4±2,1 | 15,2±0,4 | 11,5±0,7 | 13,8±0,3** |
| ИФН-γ, пг/мл | 8,8±0,8 | 6,9±0,2* | 7,2±0,4 | 6,7±0,2* |
Примечание. Различия статистически значимы (p<0,05) *— по сравнению с данными у практически здоровых; ** — между группами больных.
Согласно приведенным данным содержание ИЛ-1β, ИЛ-2 у больных СД выше, а ИНФ-γ — ниже, чем у практически здоровых лиц. Полученные нами результаты свидетельствуют об изменении локального цитокинового статуса у пациентов с различной длительностью СД-2 (>5 лет) и сиалозом. Статистически значимые различия между группами больных по длительности СД-2 отмечены по уровню ИЛ-2 (p<0,05)
Уровень гликемии по содержанию HbA1c ≤8% определялся у 22 больных сиалозом и СД-2 и в среднем в группе составил 7,2±0,1%. Недостаточный гликемический контроль (HbA1C >8%) выявлен у 18 больных и уровень HbA1c у них составил 9,0±0,2%. Статистически значимые изменения между группами отмечались по содержанию цитокинов ИЛ-1β и ИЛ-2 (p<0,05). Наиболее выраженное повышение уровня ИЛ-1β выявлено в группе с уровнем HbA1c >8,0% — среднее содержание данного цитокина составило 51,6±1,1 пг/мл и было в 1,2 раза (p<0,05) выше, чем в группе с уровнем HbA1с ≤8,0%. Повышение уровня ИЛ-2 отмечалось с такой же тенденцией, т.е. отмечалось повышение данного показателя одновременно с повышением уровня HbA1C в крови. При этом концентрация ИЛ-2 в слюне в группе с уровнем HbA1C >8,0% составила 16,7±0,7 пг/мл, что в 1,2 раза выше, чем в группе с уровнем HbA1C ≤8,0% и это изменение было статистически значимым (p<0,05; табл. 2) Уровень ИФН-γ в группе с HbA1C >8,0% составил 7,1±0,2 пг/м, что было на 4,2% выше, чем в группе с HbA1C ≤8,0%, но статистически незначимо.
Таблица 2. Сопоставление средних уровней ИЛ-1β, ИЛ-2 и ИФН-γ с уровнем гликированного гемоглобина у пациентов сиалозом и СД-2 (M±m)
Table 2. Comparison of mean IL-1β, IL-2 and FNO-γ with glycated hemoglobin level in patient with sialosis and type 2 diabetes (M±m)
| Показатель | Практически здоровые (n=10) | Уровень HbA1c | |
| ≤8,0% (n=22) | >8,0% (n=18) | ||
| ИЛ-1β, пг/мл | 42,3±3,7 | 42,3±1,1 | 51,6±1,1* ** |
| ИЛ-2, пг/мл | 11,4±2,1 | 14,1±0,3 | 16,7±0,7* ** |
| ИФН-γ, пг/мл | 8,8±0,8 | 6,8±0,3 | 7,1±0,2* |
Примечание. Различия статистически значимы (p<0,05) * — по сравнению с данными у практически здоровых; ** — между группами больных.
Таким образом, проведенные исследования показали, что недостаточный гликемический контроль у больных СД-2 и сиалозом сопровождается повышением уровня провоспалительных цитокинов в РЖ.
Весьма важной для больных СД-2 является возможность коррекции иммунных нарушений с помощью препаратов системной энзимотерапии, обладающих противоспалительными и иммуномодулирующими свойствами.
Снижение уровня ИЛ-1β в РЖ после лечения наблюдалось в двух группах больных сиалозом. Однако у пациентов основной группы после энзимотерапии содержание ИЛ-1β в РЖ было наименьшим (45,0±0,4 пг/мл) а у лиц контрольной группы составило 46,2±2,3 пг/мл.
После лечения уровень ИЛ-2 в РЖ у пациентов контрольной группы снизился незначительно с 13,6±0,3 до 13,3±0,3 пг/мл, у больных основной группы — с 13,9±0,4 до 11,9±0,2 пг/мл. В основной группе выявлено статистически значимое (p<0,05) снижение уровня ИЛ-2 в РЖ по сравнению с данными до лечения. У больных основной группы уровень ИЛ-2 в РЖ после лечения достигал почти таких же значений, как у практически здоровых (11,4±2,1 пг/мл).
У больных сиалозом на фоне СД-2 до лечения наблюдается снижение уровня ИФН-γ в РЖ и повышение его до 7,3±0,2 пг/мл после лечения в 1,1 раза (табл. 3).
Таблица 3. Содержание цитокинов в РЖ у больных сиалозом и СД-2 в динамике лечения (M±m)
Table 3. Cytokines oral fluid content in patients with sialosis and type 2 diabetes before and after treatment (M±m)
| Показатель | Практически здоровые (n=10) | Группа сравнения (n=20) | Основная группа (n=20) | ||
| до лечения | после лечения | до лечения | после лечения | ||
| ИЛ-1β, пг/мл | 45,2±4,8 | 46,3±2,5 | 46,2±2,3 | 48,4±0,8 | 45,0±0,4** |
| ИЛ-2 пг/мл | 11,4±2,1 | 13,6±0,3 | 13,3±0,3 | 13,9±0,4 | 11,9±0,2** |
| ИФН-γ пг/мл | 8,8±0,8 | 6,9±0,3* | 7,3±0,2 | 6,7±0,2* | 8,3±0,1** |
Примечание. Различия статистически значимы (p<0,05) * — по сравнению с данными у практически здоровых; ** — между группами больных после лечения.
В то же время при включении в схему лечения энзимотерапии повышение уровня ИФН-γ в основной группе было более выраженным и в среднем составило 8,3±0,1 пг/мл, что превышало исходный уровень в 1,2 раза (p<0,05).
Объективный анализ клинической картины у больных основной группы выявил улучшение общего самочувствия, усиление слюноотделения и исчезновение чувства сухости на 7-е сутки, а в контрольной группе — на 9-е сутки. Положительная динамика клинических признаков к моменту окончания лечения отмечалась у всех больных основной группы (получавших энзимотерапию) и у 14 (70%) больных контрольной группы (на фоне традиционной терапии).